Advertisements
Advertisements
Question
BF3 तथा \[\ce{BH^-_4}\] की आकृति की व्याख्या कीजिए। इन स्पीशीज़ में बोरॉन के संकरण को निर्दिष्ट कीजिए।
Solution
बोरॉन ट्राइफ्लुओराइड (Boron trifluoride, BF3) - इसमें केंद्रीय परमाणु बोरॉन है। जिसका इलेक्ट्रॉनिक विन्यास 1s2, 2s2 2p1 है। तलस्थ अवस्था में इसमें केवल एक अयुग्मित इलेक्ट्रॉन है जिसके आधार पर केवल एक सहसंयोजक बंध ही बन सकता है। अतः BF3 अणु बनने में यह अवश्य ही उत्तेजित अवस्था में होगा जिस स्थिति में एक s-इलेक्ट्रॉन p-कक्षक में उन्नत हो
जाएगा-
| 2s | 2p | ||
| आद्य अथवा तलस्थ अवस्था: | B |  |
 |
| उत्तेजित अवस्था: | B |  |
 |
उत्तेजित बोरॉन में तीन अयुग्मित इलेक्ट्रॉन हैं जिससे यह तीन सहसंयोजक बंध बना सकता है। तीन फ्लुओरीन BF3 में युग्मन के लिए तीन इलेक्ट्रॉन प्रदान करते हैं।
| 2s | 2p | |
| BF3 |  |
 |
इसमें एक बंध s-इलेक्ट्रॉन के माध्यम से है तथा अन्य दो बंध दो p-इलेक्ट्रॉनों के माध्यम से हैं। अतः तीनों बंध समान नहीं होने चाहिए। s तथा px व py कक्षकों की ऊर्जा का संचय होकर तीनों कक्षकों में बराबर राशि में वितरित हो जाता है। इस प्रकार तीन sp-संकर कक्षकों का उद्भव होता है। इन कक्षकों के बीच 120° का, कोण होता है जिससे इलेक्ट्रॉन युग्मों में पारस्परिक प्रतिकर्षण न्यूनतम रहता है।
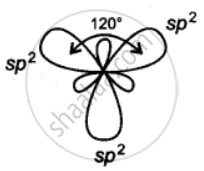
ये sp2-संकर कक्षक F परमाणुओं के कक्षकों के साथ अतिव्यापन करके बंध बनाते हैं। इस प्रकार BF3 में बंध कोण 120° होता है तथा अणु त्रिकोणीय व समतल होता है।
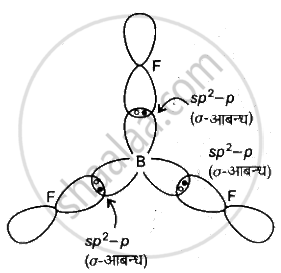
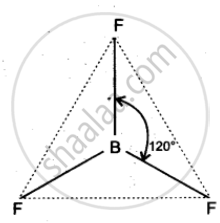
बोरॉन ट्राईफ्लुओराइड की आकृति
बोरॉन टेट्रा हाइड्राइडो ऋणायन \[\ce{(BH^-_4)}\] - वर्ग 13 के तत्व MH; प्रकार के हाइड्राइड बनाते हैं। ये हाइड्राइड दुर्बल लूइस अम्ल होते हैं तथा प्रबल लूइस क्षारकों (:B) के साथ MH3 : B प्रकार के योग उत्पाद बनाते हैं (M = B, Al, Ga)। इन हाइड्राइडों का निर्माण इनके बाह्यतम कोश में उपस्थित रिक्त । p-कक्षकों के कारण होता है जो हाइड्राइड आयन (H–) से तुरंत इलेक्ट्रॉन युग्म लेकर टेट्रा हाइड्राइडो ऋणायन बनाते हैं। \[\ce{BH^-_4}\] की संरचना संकरण के प्रकार के आधार पर निर्धारित की जा सकती है। संकरण का प्रकार निम्नलिखित सूत्र से ज्ञात किया जा सकता है-
\[\ce{H = \frac{1}{2}}\][V + M − C + A]
जहाँ H = संकरण में सम्मिलित कक्षकों की संख्या, V = केंद्रीय परमाणु के संयोजी कोश में इलेक्ट्रॉनों की संख्या, M = एकल संयोजी परमाणुओं की संख्याए, C = धनायन पर आवेश, A = ऋणायन पर आवेश इस प्रकार-
\[\ce{H = 1/2[3+4-0+1] = 4}\]
चूँकि संकरण में भाग लेने वाले कक्षकों की संख्या 4 है; अत: यह sp3 संकरण है। sp3 संकरण में एक s-कक्षक तथा तीन p-कक्षकों के सम्मिश्रण से चार समतुल्य संकर कक्षक बनते हैं। इन चारों कक्षकों में अल्पतम प्रतिकर्षण होने के लिए वे एक समचतुष्फलक के चारों कोनों की ओर दिष्ट होते हैं। तथा परस्पर 109°28′ का कोण बनाते हैं। अत: \[\ce{BH^-_4}\] की आकृति निम्नवत् होगी-
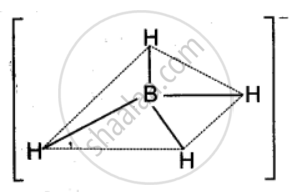
\[\ce{(BH^-4)}\] की आकृति
APPEARS IN
RELATED QUESTIONS
बोरॉन ट्राइफ्लुओराइड लूइस अम्ल के समान व्यवहार क्यों प्रदर्शित करता है?
क्या होता है, जब बोरिक अम्ल को गरम किया जाता है?
BF3 में तथा \[\ce{BF^-_4}\] में बंध लंबाई क्रमशः 130 pm तथा 143 pm होने के कारण बताइए।
डाइबोरेन की संरचना समझाइए।
बोरिक अम्ल की संरचना समझाइए।
क्या होता है, जब बोरेक्स को अधिक गरम किया जाता है?
क्या होता है, जब बोरिक अम्ल को जल में मिलाया जाता है?
बोरेक्स के जलीय विलयन की प्रकृति कौन-सी होती है?
बोरिक अम्ल के बहुलकीय होने का कारण-
डाइबोरेन में बोरॉन का संकरण कौन-सा होता है?
