Advertisements
Advertisements
प्रश्न
लैन्थेनॉयड आकुंचन क्या है?
उत्तर १
लैन्थेनॉयड की परमाणु और आयनिक त्रिज्या परमाणु संख्या में वृद्धि के साथ धीरे-धीरे कम हो जाती है। इस प्रक्रिया को लैन्थेनॉयड आकुंचन के रूप में जाना जाता है।
उत्तर २
लैन्थेनॉयड आकुंचन (Lanthanoid Contraction) – लैन्थेनॉयड श्रेणी में परमाणु क्रमांक बढ़ने पर परमाण्विक तथा आयनिक त्रिज्याएँ एक तत्व से दूसरे तत्व तक घटती हैं, परंतु यह कमी अत्यंत कम होती है।
उदाहरणार्थ – Ce से Lu तक जाने पर परमाण्विक त्रिज्या 183 pm से 173 pm तक घट जाती है तथा यह कमी केवल 10 pm है। इसी प्रकार Ce3+ से Lu3+ आयन तक जाने पर आयनिक त्रिज्या 103 pm से घटकर 85 pm रह जाती है तथा यह कमी केवल 18 pm है। अत: परमाणु क्रमांक में 14 की वृद्धि के लिए, परमाण्विक तथा आयनिक त्रिज्याओं में होने वाली कमी अत्यंत कम है। यह कमी अन्य वर्गों तथा आवर्तो के तत्वों की तुलना में अत्यल्प है।
सारणी-लैन्थेनम तथा लैन्थेनॉयडों के परमाण्विक तथा आयनिक त्रिज्याओं में परिवर्तन (pm)
| तत्व | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu |
| त्रिज्या (Ln) | 187 | 183 | 182 | 181 | 181 | 180 | 199 | 180 | 178 | 177 | 176 | 175 | 174 | 173 | - |
| त्रिज्या (Ln3+) | 106 | 103 | 101 | 99 | 98 | 96 | 95 | 94 | 92 | 91 | 89 | 88 | 87 | 85 | - |
लैन्थेनॉयड तत्वों में परमाणु क्रमांक बढ़ने पर उनके परमाणु तथा आयनिक आकारों में होने वाली स्थिर कमी ‘लैन्थेनॉयड आकुंचन’ कहलाती है।
त्रिसंयोजी लैन्थेनॉयडों (Ln3+) की आयनिक त्रिज्याओं में कमी में दर्शायी गई है।
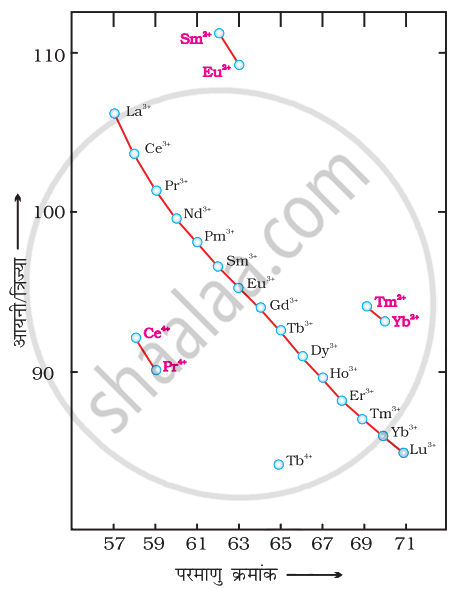
लैन्थेनॉयडों की आयनिक त्रिज्याओं में प्रवृत्तियाँ
लैन्थेनॉयड आकुंचन का कारण (Cause of Lanthanide Contraction) – लैन्थेनॉयड श्रेणी में एक तत्व से दूसरे तत्व तक जाने पर नाभिकीय आवेश एक इकाई बढ़ता है तथा एक इलेक्ट्रॉन जुड़ता है। ये नए इलेक्ट्रॉन समानान्तर 4f- उपकोशों में जुड़ते हैं। यद्यपि एक 4f- इलेक्ट्रॉन का दूसरे 4f-इलेक्ट्रॉन पर परिरक्षण प्रभाव (नाभिकीय आवेश से), f-कक्षकों के अत्यंत विस्तृत आकार के कारण, कम होता है। यद्यपि नाभिकीय आवेश प्रत्येक पद पर एक इकाई बढ़ जाता है, इसलिए परमाणु क्रमांक तथा नाभिकीय आवेश बढ़ने पर प्रत्येक 4f-इलेक्ट्रॉन द्वारा अनुभव किया जाने वाला प्रभावी नाभिकीय आवेश बढ़ जाता है, परिणामस्वरूप सम्पूर्ण 4f-इलेक्ट्रॉन कोश प्रत्येक तत्व के जुड़ने पर आकुंचित हो जाता है, यद्यपि यह कमी अत्यंत अल्प होती है। इसके परिणामस्वरूप परमाणु क्रमांक बढ़ने पर लैन्थेनॉयडों के आकार में नियमित हस पाया जाता है। क्रमिक अपचयनों का योग कुल लैन्थेनॉयड आकुंचन देता है।
APPEARS IN
संबंधित प्रश्न
निम्नलिखित के संदर्भ में लैन्थेनॉयड एवं ऐक्टिनॉयड के रसायन की तुलना कीजिए।
इलेक्ट्रॉनिक विन्यास
निम्नलिखित के संदर्भ में लैन्थेनॉयड एवं ऐक्टिनॉयड के रसायन की तुलना कीजिए।
परमाण्वीय एवं आयनिक आकार
निम्नलिखित के संदर्भ में लैन्थेनॉयड एवं ऐक्टिनॉयड के रसायन की तुलना कीजिए।
ऑक्सीकरण अवस्था
निम्नलिखित के संदर्भ में लैन्थेनॉयड एवं ऐक्टिनॉयड के रसायन की तुलना कीजिए।
रासायनिक अभिक्रियाशीलता
ऐक्टिनॉयड तत्वों का रसायन उतना नियमित नहीं है जितना कि लैन्थेनॉयड तत्वों का रसायन। इन तत्वों की ऑक्सीकरण अवस्थाओं के आधार पर इस कथन का आधार प्रस्तुत कीजिए।
लैन्थेनॉयड श्रेणी के उन सभी तत्वों का उल्लेख कीजिए जो +4 तथा जो +2 ऑक्सीकरण अवस्थाएँ दर्शाते हैं। इस प्रकार के व्यवहार तथा उनके इलेक्ट्रॉनिक विन्यास के बीच संबंध स्थापित कीजिए।
61, 91, 101 तथा 109 परमाणु क्रमांक वाले तत्वों का इलेक्ट्रॉनिक विन्यास लिखिए।
लैन्थेनॉयड धातुओं से युक्त एक प्रमुख मिश्रातु का उल्लेख कीजिए।
मिश्र धातु के उपयोग बताइए।
लैन्थेनॉयड आकुंचन के परिणाम क्या हैं?
