Advertisements
Advertisements
प्रश्न
इस अध्याय में दिए गए सभी परमाणु मॉडलों की तुलना कीजिए।
उत्तर
| I. | जे.जे.थॉमसन का परमाणु मॉडल | (i) | परमाणु धनात्मक आवेश वाले एक गोले से बना होता है जिसमें इलेक्ट्रॉन तरबूज के बीजों की तरह अंतर्निहित होते हैं। |
| (ii) |
गोले पर कुल धनात्मक आवेश, इलेक्ट्रॉनों पर उपस्थित कुल ऋणात्मक आवेश के बराबर होता है, जिससे पूरा परमाणु विद्युत रूप से उदासीन होता है। |
||
| (iii) | यह रदरफोर्ड के प्रकीर्णन प्रयोगों के परिणामों की व्याख्या नहीं कर सका। | ||
| II. | रदरफोर्ड का परमाणु मॉडल | (i) | एक परमाणु के केन्द्र में एक छोटा धनावेशित नाभिक होता है तथा इलेक्ट्रॉन उसके चारों ओर चक्कर लगाते हैं। |
| (ii) | नाभिक और इलेक्ट्रॉनों के बीच बहुत बड़ा खाली स्थान होता है। | ||
| (iii) | परमाणु का समस्त द्रव्यमान मुख्यतः नाभिक में केंद्रित होता है। | ||
| (iv) | यह परमाणु की स्थिरता की व्याख्या नहीं कर सका क्योंकि चक्कर लगाता इलेक्ट्रॉन नाभिक की ओर तेजी से बढ़ेगा। इसलिए, यह ऊर्जा खो देगा। इसकी कक्षा छोटी होती जाएगी और अंततः इलेक्ट्रॉन नाभिक में गिर जाएगा। | ||
| III. | बोर का परमाणु मॉडल | (i) | एक परमाणु के केंद्र में एक छोटा भारी धनात्मक आवेशित नाभिक होता है और इलेक्ट्रॉन इसके चारों ओर वृत्ताकार पथों में घूमते हैं जिन्हें कक्षाएँ कहते हैं। |
| (ii) |
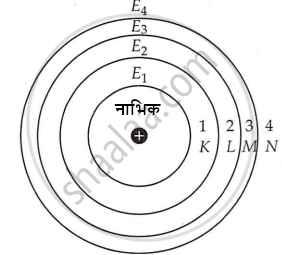
किसी विशेष परमाणु में, इलेक्ट्रॉन जिस कक्षा में घूमते हैं, वह निश्चित त्रिज्या और ऊर्जा वाली असतत कक्षाएँ होती हैं। इसलिए, इन असतत कक्षाओं को ऊर्जा स्तर या शैल भी कहा जाता है। शैल शब्द का उपयोग यह इंगित करने के लिए किया जाता है कि परमाणु त्रि-आयामी है, यानी यह प्लेट की तरह नहीं बल्कि गेंद की तरह है। चूँकि कक्षाओं की ऊर्जा निश्चित होती है, इसलिए इन्हें स्थिर अवस्थाएँ भी कहा जाता है। जैसे-जैसे हम नाभिक से बाहर की ओर बढ़ते हैं, इन्हें 1, 2, 3, 4 आदि क्रमांकित किया जाता है या इन्हें K, L, M, N आदि अक्षरों से दर्शाया जाता है, जैसा कि चित्र में दिखाया गया है। जैसे-जैसे हम नाभिक से बाहर की ओर बढ़ते हैं, इन कोशों की ऊर्जा बढ़ती जाती है। इस प्रकार, 1, 2, 3, 4 कोश आदि की ऊर्जाओं को E1, E2, E3, E4 आदि द्वारा निरूपित करने पर, हमारे पास है: E1 < E2 < E3 < E4 हालाँकि, जैसे-जैसे हम नाभिक से बाहर की ओर बढ़ते हैं, क्रमिक ऊर्जा कोशों के बीच का अंतर कम होता जाता है।
नाभिक के चारों ओर वृत्ताकार कक्षाएँ या ऊर्जा स्तर या कोश |
||
| (iii) | जब तक इलेक्ट्रॉन किसी खास कक्षा में चक्कर लगाता रहता है, तब तक वह न तो ऊर्जा खो सकता है और न ही ऊर्जा प्राप्त कर सकता है। इस प्रकार, परमाणु स्थिर रहता है और ढहता नहीं है। सबसे कम ऊर्जा वाले परमाणु की अवस्था को परमाणु की मूल अवस्था कहते हैं। | ||
| (iv) | इलेक्ट्रॉन द्वारा ऊर्जा तभी खोई या प्राप्त की जाती है जब वह एक कक्षा से दूसरी कक्षा में कूदता है। जब ऊर्जा इलेक्ट्रॉन पर पड़ती है, तो वह इस ऊर्जा को अवशोषित करता है और किसी बाहरी शेल में कूद जाता है। तब परमाणु को उत्तेजित अवस्था में कहा जाता है। उत्तेजित अवस्था में, परमाणु स्थिर नहीं होता है। यह ऊर्जा खोता है या उत्सर्जित करता है और किसी आंतरिक ऊर्जा स्तर पर वापस कूद जाता है। दूसरे शब्दों में, एक इलेक्ट्रॉन ऊर्जा को अवशोषित करके आंतरिक शेल से बाहरी शेल में कूदता है जबकि जब एक इलेक्ट्रॉन बाहरी शेल से आंतरिक शेल में कूदता है तो ऊर्जा उत्सर्जित होती है। |
APPEARS IN
संबंधित प्रश्न
कार्बन और सोडियम के परमाणुओं के लिए इलेक्ट्रॉन-वितरण लिखिए।
क्लोरीन, सल्फ़र और मैग्नीशियम की परमाणु संख्या से आप इसकी संयोजकता कैसे प्राप्त करेंगे?
उदाहरण के साथ परमाणु संख्या की व्याख्या कीजिए।
निम्नलिखित सारणी को पूरा कीजिए-
| परमाणु संख्या | द्रव्यमान संख्या | न्यूट्रॉनों की संख्या | प्रोटॉनों की संख्या | इलेक्ट्रॉनों की संख्या | परमाणु स्पीशीज़ |
| 9 | - | 10 | - | - | - |
| 16 | 32 | - | - | - | सल्फ़र |
| - | 24 | - | 12 | - | - |
| - | 2 | - | 1 | - | - |
| - | 1 | 0 | 1 | 0 | - |
निम्नलिखित में से कौन-सा कथन सर्वदा सही है?
क्या यह संभव है कि किसी तत्व के एक परमाणु में एक इलेक्ट्रॉन, एक प्रोटॉन हो और कोई न्यूट्रॉन न हो। यदि ऐसा है तो उस तत्व का नाम बताइए।
एक तत्व X के बाह्यतम कोश में 6 इलेक्ट्रॉन उपस्थित हैं। यदि यह आवश्यक इलेक्ट्रॉन ग्रहण कर उत्कृष्ट गैस का विन्यास प्राप्त करता हैतो इस प्रकार बने आयन पर कितना आवेश होगा?
एक तत्व X, जिसे `""_15^31"X"` द्वारा प्रदर्शित किया गया है, के नाभिक में उपस्थित न्यूट्रॉनों की संख्या को परिकलित कीजिए।
नीचे दिए गए प्रतीकों में उपलब्ध सूचना के आधार पर सारणी को पूर्ण कीजिए।
- `""_17^35"Cl"`
- `""_6^12"C"`
- `""_35^81"Br"`
| तत्त्व | np | nn |
सोडियम परमाणु और सोडियम आयन के इलेक्ट्रॉन वितरण को चित्र द्वारा दर्शाइए और उनके परमाणु क्रमांक भी दीजिए।