Advertisements
Advertisements
प्रश्न
कौन-सा सेल कॉपर इलेक्ट्रोड के मानक इलेक्टोड विभव का मापन करेगा?
पर्याय
Pt (s) | H2 (g, 0.1 bar) | H+ (aq., 1 M) || Cu2+ (aq., 1 M) | Cu
Pt (s) | H2 (g, 1 bar) | H+ (aq., 1 M) || Cu2+ (aq., 2 M) | Cu
Pt (s) | H2 (g, 1 bar) | H+ (aq., 1 M) || Cu2+ (aq., 1 M) | Cu
Pt (s) | H2 (g, 1 bar) | H+ (aq., 1 M) || Cu2+ (aq., 1 M) | Cu
उत्तर
Pt (s) | H2 (g, 1 bar) | H+ (aq., 1 M) || Cu2+ (aq., 1 M) | Cu
स्पष्टीकरण -
जब कॉपर इलेक्ट्रोड को मानक हाइड्रोजन इलेक्ट्रोड से जोड़ा जाता है, तो यह कैथोड के रूप में कार्य करता है और इसकी मानक इलेक्ट्रोड क्षमता को मापा जा सकता है।
`"E"^0 = "E"_"R"^0 - "E"_"L"^0 = "E"_"R"^0 - 0 = "E"_"R"^0`
दिए गए कोशिका की मानक इलेक्ट्रोड क्षमता की गणना करने के लिए इसे मानक हाइड्रोजन इलेक्ट्रोड के साथ जोड़ा जाता है जिसमें हाइड्रोजन गैस का दबाव एक बार होता है और ऑक्सीकरण और कम की सांद्रता भी होती है दाहिने हाथ में प्रजातियों के रूप अर्ध-कोशिका एकता हैं।
APPEARS IN
संबंधित प्रश्न
मैगनीशियम इलेक्ट्रोड के इलेक्ट्रोड विभव में निम्न समीकरण के अनुसार परिवर्तन होता है।
`"E"_("Mg"^(2+)|"Mg") = "E"_("Mg"^(2+)|"Mg")^Θ - (0.059)/2 log 1/(["Mg"^(2+)])`। यदि `"E"_("Mg"^(2+)|"Mg")` एवं log [Mg2+] के मध्य ग्राफ खींचे तो वह कैसा होगा ?
निम्नलिखित में से कौन-सा कथन सत्य है?
नीचे दिए गए आँकडों का प्रयोग करते हुए ज्ञात कीजिए कि अपचायक के क्रम का सही विकल्प कौन-सा है?
`"E"_("Cr"_2"O"_7^(2-)//"Cr"^(3+))^⊖`= 1.33 V `"E"_("Cl"_2//"Cl"^-)^⊖` = 1.36 V
`"E"_("MnO"_4^-//"Mn"^(2+))^⊖` = 1.51 V `"E"_("Cr"^(3+)//"Cr")^⊖` = - 0.74 V
Al2O3 से एक मोल ऐलुमिनियम प्राप्त करने के लिए आवश्यक आवेश की मात्रा है।
Cu2+/Cu मानक इलेक्ट्रोड विभव का धनात्मक मान दर्शाता है कि ______।
- यह अपोउपचायक युग्म, H+/H2 युग्म की तुलना में प्रबल अपचायक है।
- यह अपोउपचायक युग्म, H+/H2 युग्म की तुलना में प्रबल ऑक्सीकारक है।
- Cu अम्ल से H2 को विस्थापित कर सकता है।
- Cu अम्ल से H2 को विस्थापित नहीं कर सकता है।
क्या `"E"_"cell"^⊖` अथवा Δr G⊖ कभी भी शून्य के बराबर हो सकता है?
`"E"_("Zn"^(2+)//"Zn")^⊖` = - 0.76 V व्यंजक में ऋणात्मक मान से क्या तात्पर्य है?
उस गैल्वेनी सेल को चित्रित कीजिए जिसकी सेल अभिक्रिया \[\ce{Cu + 2Ag+ ⟶ 2Ag + Cu2+}\] है।
Cl- आयनों के लिए मानक इलेक्टोड विभव जल से अधिक धनात्मक है फिर भी जलीय सोडियम क्लोराइड विलयन के विद्युत अपघटन में जल की बजाए ऐनोड पर Cl आयन क्यों आक्सीकृत होता है?
चित्र पर विचार कीजिए तथा नीचे दिए गए प्रश्नों के उत्तर दीजिए।
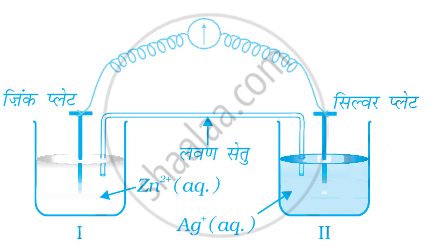
- इलेक्ट्रॉन प्रवाह की दिशा दर्शाने के लिए चित्र को पुन: बनाइए।
- सिल्वर प्लेट ऐनोड है अथवा कैथोड?
- क्या होगा यदि लवण सेतु को हटा दीया जाए?
- सेल कार्य करना कब समाप्त कर देगा?
- कार्यरत सेल में Zn2+ तथा Ag+ आयनों की सांद्रता किस प्रकार प्रभावित होगी?
- सेल समाप्त हो जाने के पश्चात Zn2+ आयनों तथा Ag+ आयनों की सांद्रता किस प्रकार प्रभावित होती है?
