Advertisements
Advertisements
Question
किसी वर्ग या आवर्त में परमाणु त्रिज्या किस प्रकार परिवर्तित होती है? इस परिवर्तन की व्याख्या आप किस प्रकार करेंगे?
Solution
आवर्त में परमाणु त्रिज्याएँ (Atomic Radii in Periods) - किसी आवर्त में बाएँ से दाएँ चलने पर परमाणु त्रिज्याएँ नियमित क्रम में क्षार धातु से हैलोजेन तक घटती हैं; क्योंकि नाभिकीय आवेश बढ़ने के साथ-साथ बाह्यतम कोश के इलेक्ट्रॉनों की संख्या भी बढ़ती है, फलस्वरूप बाह्यतम कोश के इलेक्ट्रॉनों को आकर्षित करने की क्षमता भी बढ़ती है। इस कारण इनकी नाभिक व बाह्यतमं कोशों के बीच की दूरी क्रमशः घटती है; अत: परमाणु त्रिज्या घटती है। (यह ध्यान देने योग्य है कि यहाँ उत्कृष्ट गैसों की परमाणु त्रिज्या पर विचार नहीं किया जा रहा है। एकल परमाणु होने के कारण उनकी अबंधित त्रिज्या बहुत अधिक है। इसलिए उत्कृष्ट गैसों की तुलना दूसरे तत्वों की सहसंयोजक त्रिज्या से न करके वान्डरवाल्स त्रिज्या से करते हैं।)
कुछ तत्वों के लिए परमाणु त्रिज्या का मान निम्नांकित सारणी-1 में दिया गया है-
सारणी-1: आवर्त में परमाणु त्रिज्या के मान (पीकोमीटर, pm में)
[Value of atomic radii in period (in pm)]
| परमाणु (आवर्त II) | Li | Be | B | C | N | O | F |
| परमाणु त्रिज्या | 152 | 111 | 88 | 77 | 74 | 66 | 64 |
| परमाणु (आवर्त III) | Na | Mg | Al | Si | P | S | Cl |
| परमाणु त्रिज्या | 186 | 160 | 143 | 117 | 110 | 104 | 99 |
द्वितीय आवर्त में परमाणु त्रिज्या में परमाणु क्रमांक के साथ परिवर्तन में प्रदर्शित वक्र द्वारा और अधिक स्पष्ट होता है। वक्र में स्पष्ट प्रदर्शित है कि नितांत बाईं ओर स्थित क्षार धातु (Li) की परमाणु त्रिज्या अधिकतम तथा नितांत दाईं ओर स्थित हैलोजेन (F) की परमाणु त्रिज्या का मान न्यूनतम है।
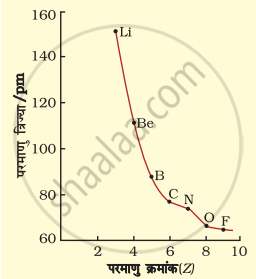
द्वितीय आवर्त में परमाणु क्रमांक के साथ तत्त्वों की परमाणु त्रिज्या में परिवर्तन
वर्ग में परमाणु त्रिज्याएँ (Atomic radii in Groups) - किसी वर्ग में ऊपर से नीचे चलने पर परमाणु त्रिज्याएँ बढ़ती हैं; क्योंकि जैसे-जैसे नाभिकीय आवेश बढ़ता है, इलेक्ट्रॉनिक कोशों की संख्या बढ़ती जाती है, फलस्वरूप बाह्यतम कोश के इलेक्ट्रॉनों को आकर्षित करने की क्षमता घटती है; अत: परमाणु त्रिज्या बढ़ती है।
निम्नांकित सारणी-2 में धातुओं तथा हैलोजेन तत्वों के लिए परमाणु त्रिज्याएँ दी गई हैं-
सारणी-2: वर्ग में परमाणु त्रिज्या के मान (पीकोमीटर, pm में)
[Values of atomic radii in groups (in pm)]
| परमाणु (वर्ग I) | परमाणु त्रिज्या | परमाणु (वर्ग 17) | परमाणु त्रिज्या |
| Li | 152 | F | 72 |
| Na | 186 | Cl | 99 |
| K | 231 | Br | 114 |
| Rb | 244 | I | 133 |
| Cs | 262 | At | 140 |
वर्ग में परमाणु क्रमांकों के साथ क्षार धातुओं तथा हैलोजेनों की परमाणु त्रिज्याओं में परिवर्तन में प्रदर्शित वक्र द्वारा और अधिक स्पष्ट होता है। मानों से यह स्पष्ट है कि लीथियम (Li) की परमाणु त्रिज्या न्यूनतम तथा सीजियम (Cs) की अधिकतम है। इसी प्रकार हैलोजेनों में फ्लुओरीन (F) की परमाणु त्रिज्या न्यूनतम तथा आयोडीन (I) की अधिकतम है।
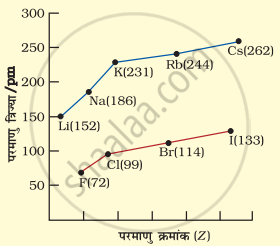
परमाणु क्रमांकों के साथ क्षारीय धातुओं तथा हैलोजेनों की परमाणु त्रिज्याओं में परिवर्तन
APPEARS IN
RELATED QUESTIONS
‘परमाणु त्रिज्या’ और ‘आयनी त्रिज्या’ से आप क्या समझते हैं?
धनायन अपने जनक परमाणुओं से छोटे क्यों होते हैं और ऋणायनों की त्रिज्या उनके जनक परमाणुओं की त्रिज्या से अधिक क्यों होती है? व्याख्या कीजिए।
उस सिद्धांत का वर्णन कीजिए, जो परमाणु की त्रिज्या से संबंधित होता है- जब वह इलेक्ट्रॉन प्राप्त करता है।
उस सिद्धांत का वर्णन कीजिए, जो परमाणु की त्रिज्या से संबंधित होता है- जब वह इलेक्ट्रॉन का त्याग करता है।
