Advertisements
Advertisements
Question
विभिन्न तापों पर N2O5 के अपघटन के लिए वेग स्थिरांक नीचे दिए गए हैं –
| T/°C | 0 | 20 | 40 | 60 | 80 |
| 105 × k/s–1 | 0.0787 | 1.70 | 25.7 | 178 | 2140 |
In k एवं 1/T के मध्य ग्राफ खींचिए तथा A एवं Ea की गणना कीजिए। 30°C तथा 50°C पर वेग स्थिरांक को प्रागुक्त कीजिए।
Solution
विभिन्न तापमानों पर N2O5 के अपघटन के दर स्थिरांक नीचे दर्शाए गए हैं।
| T(°C) | T(K) | 1/T | k(s−1) | In k (= 2.303 log k) |
| 0 | 273 | 3.6 × 10−3 | 7.87 × 10−7 | −14.06 |
| 20 | 293 | 3.4× 10−3 | 1.70 × 10−5 | −10.98 |
| 40 | 313 | 3.19 × 10−3 | 25.7 × 10−5 | −8.266 |
| 60 | 333 | 3.00 × 10−3 | 178 × 10−5 | −6.332 |
| 80 | 353 | 2.8 × 10−3 | 2140 × 10−5 | −3.844 |
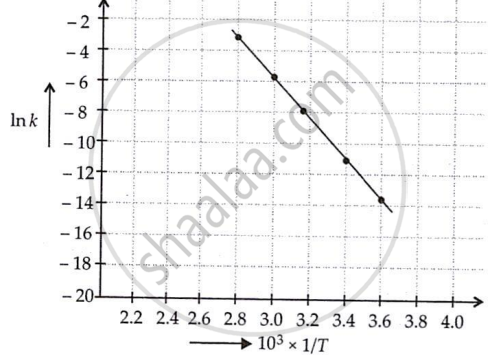
रेखा का ढलान = tan θ
= `("y"_2 - "y"_1)/("x"_2 - "x"_1)`
= `(-10.98-(-14.06))/(3.4 - 3.6) xx 10^3`
= −15.5 × 103
Ea = −ढलान × R
= −(−15.5 × 103 × 8.314)
= 128.86kJ K−1 mol−1
पुनः A में = k में + `"E"_"a"/("RT")`
= `-14.06 + (128.86 xx 10^3 "JK"^(-1) "mol"^(-1))/(8.314 xx 273)`
= −14.06 + 56.77
= 42.71
या, log A = 18.53
या, A = antilog 18.53 = 0.3388 × 1019
या, A = 3.3888 × 1018
303 K और 323 K पर दर स्थिरांक k के मान ग्राफ से प्राप्त किए जा सकते हैं।
सबसे पहले, `1/(303"K") और 1/(323"K")` के अनुरूप k प्राप्त किया जाता है और फिर k की गणना की जाती है।
APPEARS IN
RELATED QUESTIONS
10°C ताप पर A के उत्पाद में विघटन के लिए k का मान 4.5 × 103 s−1 तथा सक्रियण ऊर्जा 60 kJ mol−1 है। किस ताप पर k का मान 1.5 × 104 s−1 होगा?
ताप में 293 K से 313 K तक वृद्धि करने पर किसी अभिक्रिया का वेग चार गुना हो जाता है। इस अभिक्रिया के लिए सक्रियण ऊर्जा की गणना यह मानते हुए कीजिए कि इसका मान ताप के साथ परिवर्तित नहीं होता।
निम्नलिखित में से कौन-सा ग्राफ ऊष्माक्षेपी अभिक्रिया को प्रदर्शित करता है-
(क)
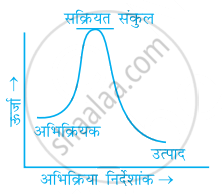
(ख)
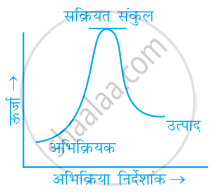
(ग)
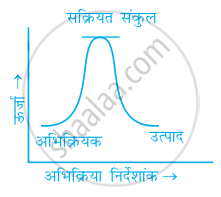
उत्प्रेरक के लिए निम्नलिखित में से कौन-सा कथन सही कथन नहीं है?
निम्नलिखित में से कौन-सा कथन अरेनियस समीकरण के अनुसार है?
- ताप में वृद्धि के साथ अभिक्रिया का वेग बढता है।
- सक्रियण ऊर्जा में कमी के साथ अभिक्रिया का वेग बढ़ता है।
- ताप में वृद्धि के साथ वेग स्थिरांक में चरघतांकी कमी होती है।
- सक्रियण ऊर्जा में कमी से अभिक्रिया का वेग घटता है।
अभिक्रिया में अणुओं के बहुत बड़े अंश की ऊर्जा देहली ऊर्जा से अधिक है फिर भी अभिक्रिया वेग बहुत कम है, ऐसा क्यों है?
तीन से अधिक आणिकता वाली अभिक्रियाओं की संभावनाएँ बहुत कम क्यों होती हैं?
सामान्यत:, अभिक्रिया के दौरान अभिक्रिया वेग घटता क्यों है?
किसी अभिक्रिया के लिए केवल ऊष्मागतिक संभाव्यता अभिक्रिया के वेग को निर्धारित नहीं कर सकती। इसे एक उदाहरण की सहायता से समझाइए।
ऑक्सैलिक अम्ल तथा KMnO4 के मध्य ऑक्सीकरण-अपचयन अनुमापन में हम अनुमापन प्रारम्भ करने से पूर्व ऑक्सैलिक अम्ल विलयन को गरम क्यों करते हैं?
