Advertisements
Advertisements
प्रश्न
अष्टक नियम के महत्त्व और सीमाओं को लिखिए।
उत्तर
अष्टक नियम का महत्त्व (Significance of Octet Rule) अष्टक नियम अत्यन्त उपयोगी है। इसका महत्त्व निम्नवर्णित है-
- अधिकांश अणु अष्टक नियम का अनुसरण करके ही निर्मित होते हैं; जैसे- O2, N2, Cl2, Br2, आदि।
- अधिकांश कार्बनिक यौगिकों की संरचनाओं को समझने में अष्टक नियम का अत्यधिक महत्त्व है।
- इसे मुख्य रूप से आवर्त सारणी के द्वितीय आवर्त के तत्वों पर लागू किया जा सकता है।
अष्टक नियम की सीमाएँ (Limitations of Octet Rule) यद्यपि अष्टक नियम अत्यंत उपयोगी है, परंतु यह सदैव लागू नहीं किया जा सकता अर्थात् यह सार्वत्रिक (universal) नहीं है। अष्टक नियम के तीन प्रमुख अपवाद निम्नलिखित हैं-
(1) केंद्रीय परमाणु का अपूर्ण अष्टक (Incomplete octet of central atom) - कुछ यौगिकों में केंद्रीय परमाणु के चारों ओर उपस्थित इलेक्ट्रॉनों की संख्या आठ से कम होती है। यह मुख्यत: उन तत्त्वों के यौगिकों में होता है जिनमें संयोजकता इलेक्ट्रॉनों की संख्या चार से कम होती है। उदाहरण के लिए- LiCl2BeH2 तथा BCl3 के बनने में,
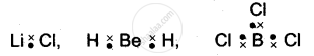
Li, Be तथा B के संयोजकता इलेक्ट्रॉनों की संख्या क्रमशः 1, 2 तथा 3 हैं। इस प्रकार के अन्य उदाहरण AICl3 तथा BF; हैं।
(2) विषम इलेक्ट्रॉन अणु (Odd electron molecule) - उन अणुओं, जिनमें इलेक्ट्रॉनों की कुल संख्या विषम (odd) होती है; जैसे-नाइट्रिक ऑक्साइड (NO) तथा नाइट्रोजन डाइऑक्साइड (NO2) में सभी परमाणु अष्टक नियम का पालन नहीं कर पाते।

(3) प्रसारित अष्टक (Expanded octet) - आवर्त सारणी के तीसरे तथा इससे आगे के आवर्ती के तत्वों में आबंधन के लिए 3s तथा 3p-कक्षकों के अतिरिक्त 3d-कक्षक भी उपलब्ध होते हैं। इन तत्त्वों के अनेक यौगिकों में केंद्रीय परमाणु के चारों ओर आठ से अधिक इलेक्ट्रॉन होते हैं। इसे प्रसारित अष्टक (expanded octet) कहते हैं। स्पष्ट है कि इन यौगिकों पर अष्टक नियम लागू नहीं होता है। ऐसे यौगिकों के कुछ उदाहरण हैं- PF5, SF6, H2SO4 तथा कई उपसहसंयोजक यौगिक।
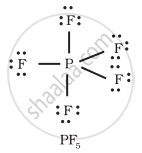
P परमाणु के चारों ओर 10 इलेक्ट्रॉन हैं।
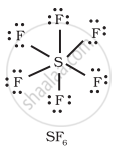
S परमाणु के चारों ओर 12 इलेक्ट्रॉन हैं।
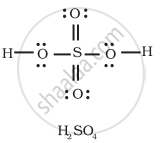
S परमाणु के चारों ओर 12 इलेक्ट्रॉन हैं।
APPEARS IN
संबंधित प्रश्न
निम्नलिखित तत्त्वों के परमाणुओं के लूइस बिंदु प्रतीक लिखिए-
Mg, Na, B, O, N, Br
निम्नलिखित अणु तथा आयन की लूइस संरचनाएँ लिखिए-
H2S
निम्नलिखित परमाणुओं से इलेक्ट्रॉन स्थानांतरण द्वारा धनायनों तथा ऋणायनों में विरचन को लूइस बिंदु-प्रतीकों की सहायता से दर्शाइए-
K तथा S
निम्नलिखित परमाणुओं से इलेक्ट्रॉन स्थानांतरण द्वारा धनायनों तथा ऋणायनों में विरचन को लूइस बिंदु-प्रतीकों की सहायता से दर्शाइए-
Al तथा N
विद्युत-ऋणात्मकता को परिभाषित कीजिए।
विद्युत-ऋणात्मकता इलेक्ट्रॉन बंधुता से किस प्रकार भिन्न है?
निम्नलिखित परमाणु तथा आयन के लूइस बिंदु प्रतीक लिखिए।
AI और Al3+
निम्नलिखित अणु तथा आयन की लूइस संरचनाएँ लिखिए-
SiCl4
निम्नलिखित अणु तथा आयन की लूइस संरचनाएँ लिखिए-
BeF2
निम्नलिखित अणु तथा आयन की लूइस संरचनाएँ लिखिए-
\[\ce{CO^{2-}3}\]
