Advertisements
Advertisements
प्रश्न
[Cr(NH3)6]3+ अनुचुंबकीय है, जबकि [Ni(CN)4]2− प्रतिचुंबकीय, समझाइए क्यों?
उत्तर
[Cr(NH3)6]3+ का निर्माण: [Cr(NH3)6]3+ आयन में क्रोमियम की ऑक्सीकरण अवस्था +3 है। क्रोमियम का इलेक्ट्रॉनिक विन्यास [Ar] 3d54s1 है। संकरण को निम्नलिखित आरेख में दर्शाया गया है –
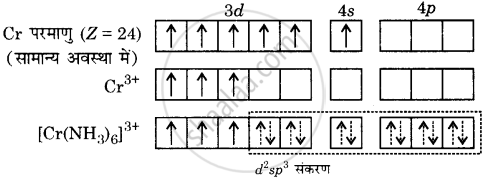
Cr3+ आयन अमोनिया के छह अणुओं से छह इलेक्ट्रॉन युग्मों को स्थान देने के लिए छह रिक्त कक्षक उपलब्ध कराते हैं। परिणामत: संकुल [Cr(NH3)6]3+ में d2sp3 संकरण होता है तथा यह अष्टफलकीय होता है। संकुल में तीन अयुग्मित इलेक्ट्रॉनों की उपस्थिति इसके अनुचुंबकीय गुण को स्पष्ट करती हैं।
[Ni(CN)4]2− का निर्माण: [Ni(CN)4]2− में Ni की ऑक्सीकरण अवस्था +2 है तथा इसका इलेक्ट्रॉनिक विन्यास 3d है। संकरण को निम्नवत् समझाया जा सकता है –
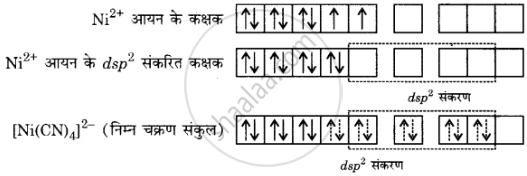
प्रत्येक संकरित कक्षक सायनाइड आयन से एक इलेक्ट्रॉन युग्म ग्रहण करता है। अयुग्मित इलेक्ट्रॉनों की अनुपस्थिति [Ni(CN)4]2− के प्रतिचुंबकीय व्यवहार की पुष्टि करती है।
APPEARS IN
संबंधित प्रश्न
संयोजकता आबंध सिद्धांत के आधार पर समझाइए कि वर्ग समतलीय संरचना वाला [Ni(CN)4]2− आयन प्रतिचुंबकीय है तथा चतुष्फलकीय ज्यामिति वाला [NiCl4]2− आयन अनुचुंबकीय है।
[NiCl4]2− अनुचुंबकीय है, जबकि [Ni(CO)4] प्रतिचुंबकीय है यद्यपि दोनों चतुष्फलकीय हैं। क्यों?
वर्ग समतली (Pt(CN)4]2− आयन में अयुग्मित इलेक्ट्रॉनों की संख्या बतलाइए।
संयोजकता आबंध सिद्धांत के आधार पर निम्नलिखित उपसहसंयोजन सत्ता में आबंध की प्रकृति की विवेचना कीजिए –
[Fe(CN)6]4−
संयोजकता आबंध सिद्धांत के आधार पर निम्नलिखित उपसहसंयोजन सत्ता में आबंध की प्रकृति की विवेचना कीजिए –
[FeF6]3−
निम्नलिखित अणु में सिग्मा (σ) तथा पाई (π) आबंधों की कुल संख्या कितनी है?
C2H2
निम्नलिखित अणु में सिग्मा (σ) तथा पाई (π) आबंधों की कुल संख्या कितनी है?
C2H4
x-अक्ष को अंतर्नाभिकीय अक्ष मानते हुए बताइए कि निम्नलिखित में कौन-से कक्षक सिग्मा (σ) आबंध नहीं बनाएँगे और क्यों?
(क) 1s तथा 1s
(ख) 1s तथा 2px
(ग) 2py तथा 2py
(घ) 1s तथा 2s
सिग्मा तथा पाई आबंध में अंतर स्पष्ट कीजिए।
संयोजकता आबंध सिद्धांत के आधार पर H2 अणु के विरचन की व्याख्या कीजिए।
