Advertisements
Advertisements
प्रश्न
संयोजकता आबंध सिद्धांत के आधार पर निम्नलिखित उपसहसंयोजन सत्ता में आबंध की प्रकृति की विवेचना कीजिए –
[Fe(CN)6]4−
उत्तर
इस संकुल आयन में आयरन की ऑक्सीकरण अवस्था +2 है।
Fe का इलेक्ट्रॉनिक विन्यास = [Ar] 3d64s2
Fe2+ का इलेक्ट्रॉनिक विन्यास = [Ar] 3d6
छह सायनाइड आयनों से छह इलेक्ट्रॉन युग्मों को स्थान देने के लिए आयरन (II) आयन को छह रिक्त कक्षक उपलब्ध करने चाहिए। ऐसा निम्नलिखित संकरण पद्धति के द्वारा प्राप्त किया जा सकता है जिसमें d-उपकोश के इलेक्ट्रॉन युग्मित हो जाते हैं, चूँकि CN– आयन प्रबल क्षेत्र लिगन्ड हैं।
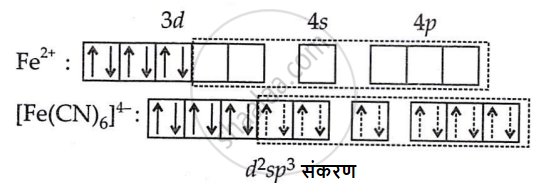
अत: छह सायनाइड आयनों से छह इलेक्ट्रॉन युग्म आयरन (II) आयन के छह संकरित कक्षकों को अध्यासित कर लेते हैं। इस प्रकार किसी भी कक्षक में अयुग्मित इलेक्ट्रॉन नहीं होते हैं, इसलिए [Fe(CN)6]4− प्रतिचुंबकत्व दर्शाता है। अतः [Fe(CN)6]4− प्रतिचुंबकीय तथा अष्टफलकीय है।
APPEARS IN
संबंधित प्रश्न
संयोजकता आबंध सिद्धांत के आधार पर समझाइए कि वर्ग समतलीय संरचना वाला [Ni(CN)4]2− आयन प्रतिचुंबकीय है तथा चतुष्फलकीय ज्यामिति वाला [NiCl4]2− आयन अनुचुंबकीय है।
वर्ग समतली (Pt(CN)4]2− आयन में अयुग्मित इलेक्ट्रॉनों की संख्या बतलाइए।
संयोजकता आबंध सिद्धांत के आधार पर निम्नलिखित उपसहसंयोजन सत्ता में आबंध की प्रकृति की विवेचना कीजिए –
[FeF6]3−
संयोजकता आबंध सिद्धांत के आधार पर निम्नलिखित उपसहसंयोजन सत्ता में आबंध की प्रकृति की विवेचना कीजिए –
[Co(C2O4)3]3−
[Cr(NH3)6]3+ अनुचुंबकीय है, जबकि [Ni(CN)4]2− प्रतिचुंबकीय, समझाइए क्यों?
ध्रुवीय सहसंयोजी आबंध से आप क्या समझते हैं? उदाहरण सहित व्याख्या कीजिए।
निम्नलिखित अणु में सिग्मा (σ) तथा पाई (π) आबंधों की कुल संख्या कितनी है?
C2H2
x-अक्ष को अंतर्नाभिकीय अक्ष मानते हुए बताइए कि निम्नलिखित में कौन-से कक्षक सिग्मा (σ) आबंध नहीं बनाएँगे और क्यों?
(क) 1s तथा 1s
(ख) 1s तथा 2px
(ग) 2py तथा 2py
(घ) 1s तथा 2s
इलेक्ट्रॉनों के आबंधी युग्म तथा एकाकी युग्म से आप क्या समझते हैं? प्रत्येक के एक उदाहरण द्वारा स्पष्ट कीजिए।
संयोजकता आबंध सिद्धांत के आधार पर H2 अणु के विरचन की व्याख्या कीजिए।
