Advertisements
Advertisements
Question
निम्नलिखित अणुओं की आकृति की व्याख्या वी. एस. ई. पी. आर. सिद्धांत के अनुरूप कीजिए-
BeCl2, BCl3, SiCl4, AsF5, H2S, PH3
Solution
१. BeCl2: केंद्रीय Be परमाणु में केवल 2 आबंध युग्म हैं तथा कोई एकाकी युग्म नहीं (Cl: Be: C) है। अत: इसकी आकृति रेखीय (linear) होगी।
२. BCl3: केंद्रीय बोरोन परमाणु में केवल 3 आबंध युग्म हैं तथा कोई एकाकी युग्म नहीं है।

अत: इसकी आकृति त्रिकोणीय समतलीय (trigonal planar) होगी।
३. SiCl4: केंद्रीय सिलिकॉन परमाणु में 4 आबंध युग्म हैं तथा कोई एकाकी युग्म नहीं है।
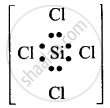
अत: इसकी आकृति चतुष्फलकीय (tetrahedral) होगी।
४. AsF5: केंद्रीय ऑसेनिक परमाणु में 5 आबंध युग्म हैं तथा कोई एकाकी युग्म नहीं है।

अत: इसकी आकृति त्रिभुजाकार द्विपिरामिडीय है।
५. H2S: केंद्रीय सल्फर परमाणु में 2 आबंध युग्म हैं तथा कोई एकाकी युग्म नहीं है।
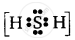
अतः इसकी आकृति बंकित (bent) होगी।
६. PH3: केंद्रीय फॉस्फोरस परमाणु में 3 आबंध युग्म हैं और एक एकाकी युग्म है।
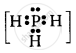
अत: इसकी आकृति त्रिकोणीय समतलीय (trigonal planar) होगी।
