Advertisements
Advertisements
Question
\[\ce{2A + B -> C + D}\] अभिक्रिया की बलगतिकी अध्ययन करने पर निम्नलिखित परिणाम प्राप्त हुए। अभिक्रिया के लिए वेग नियम तथा वेग स्थिरांक ज्ञात कीजिए।
| प्रयोग | [A]/mol L−1 | [B]/mol L−1 | D के विरचन का प्रारंभिक वेग/mol L−1 min−1 |
| I | 0.1 | 0.1 | 6.0 × 10−3 |
| II | 0.3 | 0.2 | 7.2 × 10−2 |
| III | 0.3 | 0.4 | 2.88 × 10−1 |
| IV | 0.4 | 0.1 | 2.40 × 10−2 |
Solution
प्रयोग I तथा IV में [B] समान है लेकिन [A] चार गुना हो गया है तथा अभिक्रिया का वेग भी चार गुना हो गया है।
∴ A के सापेक्ष वेग `∝` [A] …..(i)
प्रयोग II तथा III में [A] समान है लेकिन [B] दोगुना हो गया है तथा अभिक्रिया का वेग I भी चार गुना हो गया है।
B के सापेक्ष वेग `∝` [B]2 …..(ii)
समीकरण (i) तथा (ii) को संयुक्त करने पर हमें अभिक्रिया \[\ce{2A + B -> C + D}\] का वेग नियम प्राप्त हो जाता है।
वेग = k [A] [B]2
अभिक्रिया की समग्र कोटि = 1 + 2 = 3
वेग स्थिरांक की गणना:
k = `"वेग"/(["A"]["B"]^2)`
= `("mol L"^-1 "min"^-1)/(("mol L"^-1)("mol L"^-1)^2)`
= mol−2 L2 min−1
kI = `(6.0 xx 10^-3)/(0.1 xx (0.1)^2)` = 6.0
kII = `(7.2 xx 10^-2)/(0.3 xx (0.2)^2)` = 6.0
kIII = `(2.88 xx 10^-1)/(0.3 xx (0.4)^2)` = 6.0
kIV = `(2.4 xx 10^-2)/(0.4 xx (0.1)^2)` = 6.0
अतः वेग स्थिरांक = 6.0 mol−2 L2 min−1
APPEARS IN
RELATED QUESTIONS
\[\ce{R -> P}\], अभिक्रिया के लिए अभिकारक की सांद्रता 0.03 M से 25 मिनट में परिवर्तित होकर 0.02 M हो जाती है। औसत वेग की गणना सेकेंड तथा मिनट दोनों इकाइयों में कीजिए।
\[\ce{2A -> {उत्पाद}}\], अभिक्रिया में A की सांद्रता 10 मिनट में 0.5 mol L−1 से घटकर 0.4 mol L−1 रह जाती है। इस समयांतराल के लिए अभिक्रिया वेग की गणना कीजिए।
डाइमेथिल ईथर के अपघटन से CH4, H2 तथा CO बनते हैं। इस अभिक्रिया का वेग निम्नलिखित समीकरण द्वारा दिया जाता है –
वेग = k [CH3OCH3]3/2
अभिक्रिया के वेग का अनुगमन बंद पात्र में बढ़ते दाब द्वारा किया जाता है, अतः वेग समीकरण को डाइमेथिल ईथर के आंशिक दाब के पद में भी दिया जा सकता है। अतः
वेग = `k(P_(CH_3OCH_3))^(3/2)`
यदि दाब को bar में तथा समय को मिनट में मापा जाए तो अभिक्रिया के वेग एवं वेग स्थिरांक की इकाइयाँ क्या होंगी?
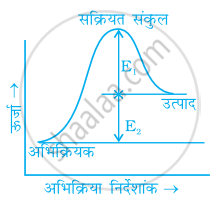
रासायनिक अभिक्रिया की सक्रियण ऊर्जा को ______ निर्धारित किया जा सकता है।
चित्र पर विचार कीजिए और सही विकल्प को चिहित कीजिए।
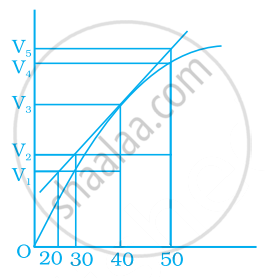
जिंक और तनु HCl की अभिक्रिया में बनी हाइड्रोजन के आयतन और समय के मध्य ग्राफ चित्र में दिया है। इसके आधार पर सही उत्तर पर निशान लगाइए।
रासायनिक अभिक्रियाओं के संघट्ट सिद्धांत के संबंध में निम्नलिखित में से कौन-सा कथन गलत है?
एक ऐसी परिस्थिति बताइए जिसमें द्विअणुक अभिक्रिया गतिक रूप से प्रथम कोटि की अभिक्रिया हो।
कॉलम I और कॉलम II में दिए कथनों को सुमेलित कीजिए।
| कॉलम I | कॉलम II |
| (i) उत्प्रेरक अभिक्रिया के वेग को | (a) भिन्नात्मक अथवा शून्य नहीं हो सकती परिवर्तित कर देते हैं। |
| (ii) आण्विकता | (b) हमेशा उपयुक्त अभिविन्यास नहीं होता। |
| (iii) प्रथम कोटि अभिक्रिया की द्वितीय अर्धआयु | (c) सक्रियण ऊर्जा को कम करके |
| (iv) `"e"^(- "E"_"a"//"RT")` | (d) प्रथम के समान होती है। |
| (v) ऊर्जा की दृष्टि से अनुकूल अभिक्रिया कभी-कभी धीमी होती है। | (e) कुल प्रायिकता एक है। |
| (vi) मैक्सवेल बोल्ट्जमान वक्र के अंतर्गत क्षेत्रफल | (f) सक्रियण ऊर्जा के बराबर अथवा उससे स्थिर होता है। अधिक ऊर्जा वाले अणुओं के अंश से संबंधित |
तत्क्षण वेग और औसत वेग में अन्तर स्पष्ट कीजिए।
