Advertisements
Chapters
2: विलयन
3: विद्युत् रसायन
▶ 4: रासायनिक बलगतिकी
5: पृष्ठ रसायन
Chapter 6: तत्वों के पृथक्करण के सामान्य सिद्धांत एवं प्रक्रम
Chapter 7: p-ब्लॉक तत्व
Chapter 8: d-एवं f-ब्लॉक तत्व
9: उपसहसंयोजन यौगिक
10: हैलोऐल्केन तथा हैलोऐरीन
11: ऐल्कोहॉल, फ़ीनॉल एवं ईथर
Chapter 12: ऐल्डिहाइड, कीटोन एवं कार्बोकिसलिक अम्ल
Chapter 13: ऐमीन
Chapter 14: जैव अणु
Chapter 15: बहुलक
Chapter 16: दैनिक जीवन मे रसायन
![NCERT Exemplar solutions for Chemistry [Hindi] Class 12 chapter 4 - रासायनिक बलगतिकी NCERT Exemplar solutions for Chemistry [Hindi] Class 12 chapter 4 - रासायनिक बलगतिकी - Shaalaa.com](/images/chemistry-hindi-class-12_6:5f2b1b2038084cf381bfa42c826a928c.jpg)
Advertisements
Solutions for Chapter 4: रासायनिक बलगतिकी
Below listed, you can find solutions for Chapter 4 of CBSE NCERT Exemplar for Chemistry [Hindi] Class 12.
NCERT Exemplar solutions for Chemistry [Hindi] Class 12 4 रासायनिक बलगतिकी अभ्यास [Pages 49 - 61]
बहुविकल्प प्रश्न (प्ररूप - I)
उत्प्रेरक परिवर्तित करते हैं-
अभिक्रिया की गिब्ज़ ऊर्जा
अभिक्रिया की एन्थेल्पी
अभिक्रिया की सक्रियण ऊर्जा
साम्यावस्था स्थिरांक
उत्प्रेरक की उपस्थिति में, अभिक्रिया के दौरान ऊष्मा का अवशोषण अथवा उत्सर्जन ______।
बढता है।
घटता है।
अपरिवर्तित रहता है।
बढ़ अथवा घट सकता है।
रासायनिक अभिक्रिया की सक्रियण ऊर्जा को ______ निर्धारित किया जा सकता है।
मानक ताप पर वेग नियतांक का निर्धारण करके
दो तापों पर वेग नियंताकों का निर्धारण करके
संघट्ट की प्रायिकता का निर्धारण करके
उत्प्रेरक का उपयोग कर
चित्र पर विचार कीजिए और सही विकल्प को चिहित कीजिए।
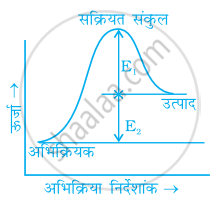
अग्र अभिक्रिया की सक्रियण ऊर्जा E1 + E2 है और उत्पाद अभिक्रियक से कम स्थायी है।
अग्र अभिक्रिया की सक्रियण ऊर्जा E1 + E2 है और उत्पाद अभिक्रियकों से अधिक स्थायी है।
अग्र और पश्च दोनों अभिक्रियाओं की सक्रियण ऊर्जा E1 + E2 है और अभिक्रियक उत्पाद से अधिक स्थायी है।
पश्च अभिक्रिया की सक्रियण ऊर्जा E1 है तथा उत्पाद अभिक्रियक से स्थायी हैं।
नीचे दी गई गैस प्रावस्था में प्रथम कोटि की विघटन अभिक्रिया पर विचार कीजिए।
\[\ce{A(g) -> B(g) + C{g}}\]
A के विघटन से पूर्व तंत्र का प्रारंभिक दाब pi था। 't' समय के पश्चात तंत्र का दाब x इकाई बढ़ कर pt हो जाता है। अभिक्रिया के लिए वेग स्थिरांक k को लिखा जा सकता है-
κ = `(2.303)/"t" log "p"_"i"/("p"_"i" - x)`
κ = `(2.303)/"t" log "p"_"i"/("2p"_"i" - "p"_"t")`
κ = `(2.303)/"t" log "p"_"i"/("2p"_"i" + "p"_"t")`
κ = `(2.303)/"t" log "p"_"i"/("p"_"i" + x)`
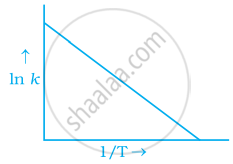
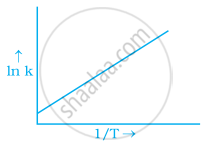
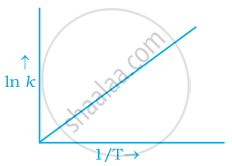
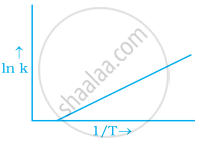
अरेनिअस समीकरण के अनुसार `"Ae"^(−"E"_"a"//"RT")` अभिक्रिया दर स्थिरांक k के बराबर है। ln k और `1/"T"` के मध्य ग्राफ को निम्न विकल्पों में से किसके द्वारा प्रदर्शित किया जा सकता है।
निम्नलिखित अरेनियस समीकरण पर विचार कीजिए और सही विकल्प पर निशान लगाइए।
κ = `"Ae"^(-"E"_"a"//"RT")`
अभिक्रिया स्थिरांक बढุती सक्रियण ऊर्जा और घटते ताप के साथ चरघातांक से बढ़ता है।
अभिक्रिया स्थिरांक बढุती सक्रियण ऊर्जा और घटते ताप के साथ चरघातांक से कम होता है।
अभिक्रिया दर स्थिरांक घटती सक्रियण ऊर्जा और घटते ताप के साथ चरघातांक से बढ़ता है।
अभिक्रिया दर स्थिरांक घटती सक्रियण ऊर्जा और बढ़ते ताप के साथ चरघातांक से बढ़ता है।
जिंक और तनु HCl की अभिक्रिया में बनी हाइड्रोजन के आयतन और समय के मध्य ग्राफ चित्र में दिया है। इसके आधार पर सही उत्तर पर निशान लगाइए।
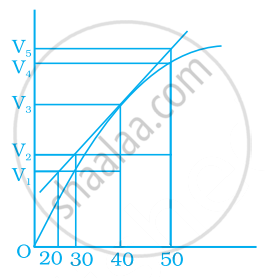
40 सेकंड तक औसत दर है `("V"_3 - "V"_2)/40`
40 सेकंड तक औसत दर है `("V"_3 - "V"_2)/(40 - 30)`
40 सेकंड तक औसत दर है `"V"_3/40`
40 सेकंड तक औसत दर है `("V"_3 - "V"_1)/(40 - 20)`
अभिक्रिया की कोटि के बारे में कौन-सा कथन सही नहीं है?
अभिक्रिया की कोटि एक भिन्नांक हो सकती है।
अभिक्रिया की कोटि का निर्धारण प्रयोग द्वारा किया जाता है।
अभिक्रिया की कोटि सदैव अभिक्रिया के लिए संतुलित रासायनिक समीकरण में अभिक्रियकों के स्टॉइकियोमीट्री गुणांकों का योग होती है।
अभिक्रिया की कोटि वेग व्यंजक में अभिक्रियकों की मोलर सांद्रताओं के घातांकों के योग के बराबर होती है।
चित्र पर विचार कीजिए। निम्नलिखित में से कौन-सा विकल्प चालीसवें सेकेंड पर तात्षणिक वेग नहीं दर्शाता?

`("V"_5 - "V"_2)/(50 - 30)`
`("V"_4 - "V"_2)/(50 - 30)`
`("V"_3 - "V"_2)/(40 - 30)`
`("V"_3 - "V"_1)/(40 - 20)`
निम्नलिखित में से कौन-सा कथन सही है?
अभिक्रिया की दर समय व्यतीत होने के साथ कम होती जाती है क्योंकि अभिक्रियकों की सांद्रता कम होने लगती है।
अभिक्रिया की दर अभिक्रिया के दौरान हर समय एक सी रहती है।
अभिक्रिया की दर ताप परिवर्तन पर निर्भर नहीं करती।
अभिक्रियकों की सांद्रता बढ़ाने से अभिक्रिया का दर कम हो जाती है।
नीचे दी गई अभिक्रिया की अभिक्रिया दर के लिए निम्नलिखित व्यंजकों में से कौन-सा सही है?
\[\ce{5Br^- (aq) + BrO3^- (aq) + 6H^+ (aq) -> 3Br2 (aq) + 3H2O(l)}\]
`(∆["Br"^-])/(∆"t") = 5 (∆["H"^+])/(∆"t")`
`(∆["Br"^-])/(∆"t") = 6/5 (∆["H"^+])/(∆"t")`
`(∆["Br"^-])/(∆"t") = 5/6 (∆["H"^+])/(∆"t")`
`(∆["Br"^-])/(∆"t") = 6 (∆["H"^+])/(∆"t")`
निम्नलिखित में से कौन-सा ग्राफ ऊष्माक्षेपी अभिक्रिया को प्रदर्शित करता है-
(क)
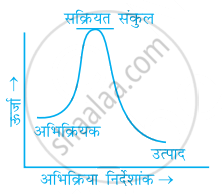
(ख)
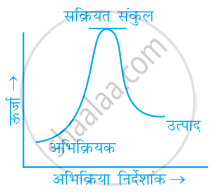
(ग)
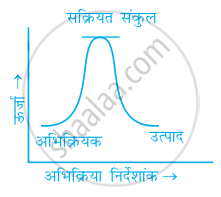
केवल (क)
केवल (ख)
केवल (ग)
(क) और (ख)
अभिक्रिया A + 2B ⟶ C के लिए निम्नलिखित वेग नियम प्राप्त होता है। बेग = k [A][B]
'A' की सांद्रता स्थिर रखते हुए अभिक्रियक 'B' की सांद्रता दुगनी करने पर वेग नियतांक का मान ______।
समान रहेगा
दुगना हो जाएगा
चार गुना हो जाएगा
आधा रह जाएगा
रासायनिक अभिक्रियाओं के संघट्ट सिद्धांत के संबंध में निम्नलिखित में से कौन-सा कथन गलत है?
यह अभिक्रिया करने वाले अणुओं अथवा परमाणुओं को कठोर गोले मानता है और उनके संरचनात्मक गुणों पर ध्यान नहीं देता।
प्रभावी संघट्टों की संख्या अभिक्रिया दर निर्धारित करती है।
उत्पाद पर्याप्त देहली ऊर्जा प्राप्त अणुओं अथवा परमापुओं के संघट्ट के परिणामस्वरूप बनते हैं।
संघट्ट के प्रभावी होने के लिए अणुओं को पर्याप्त देहली ऊर्जा और उचित अभिविन्यास के साथ टकराना चाहिए।
एक प्रथम कोटि की अभिक्रिया 1.26 × 1014s में 50% पूर्ण होती है। 100% पूर्ण होने में इसे कितना समय लगेगा?
1.26 × 1015s
2.52 × 1014s
2.52 × 1028s
अनन्त
यौगिक 'A' और 'B' निम्नलिखित रासायनिक समीकरण के अनुसार अभिक्रिया करते हैं।
\[\ce{A(g) + 2B(g) -> 2C(g)}\]
किसी एक अभिक्रियक की सांद्रता स्थिर रखते हुए 'A' अथवा 'B' की सांद्रता में परिवर्तन किया गया और वेग को प्रारंभिक संद्रता के कारक के रूप में मापा गया। निम्नलिखित परिणाम प्राप्त हुए। इस अभिक्रिया के वेग समीकरण के लिए सही विकल्प चुनिए।
| प्रयोग | [A] की प्रारंभिक सांद्रता/mol L-1 |
[B] की प्रारंभिक सांद्रता/mol L-1 |
[C] के बनने की प्रारंभिक दर/mol L-1 s-1 |
| 1. | 0.30 | 0.30 | 0.10 |
| 2. | 0.30 | 0.60 | 0.40 |
| 3. | 0.60 | 0.30 | 0.20 |
दर = κ [A]2[B]
दर = κ [A] [B]2
दर = κ [A] [B]
दर = κ [A]2 [B]0
उत्प्रेरक के लिए निम्नलिखित में से कौन-सा कथन सही कथन नहीं है?
यह अग्र और पश्च दोनों अभिक्रियाओं को समान रूप से उत्रेरित करता है।
यह अभिक्रिया का ΔG परिवर्तित कर देता है।
यह वह पदार्थ है जो अभिक्रिया के साम्यस्थिरांक को परिवर्तित नहीं करता।
यह अभिक्रियकों और उत्पादों की सक्रियण ऊर्जा को कम करके वैकल्पिक क्रियाविधि देता है।
एक छद्म प्रथम कोटि की अभिक्रिया के लिए वेग स्थिरांक का मान ______।
अल्प मात्रा में उपस्थित अभिक्रियकों की सांद्रता पर निर्भर करता है।
आधिक्य में उपस्थित अभिक्रियकों की सांद्रता पर निर्भर करता है।
अभिक्रियकों की सांद्रता पर निर्भर नहीं करता है।
केवल ताप पर निर्भर करता है।
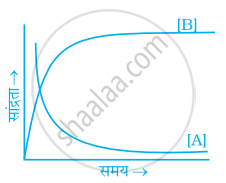
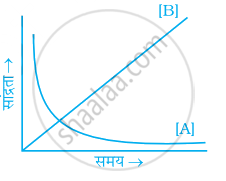
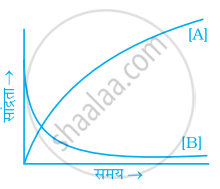
अभिक्रिया A ⇌ B पर विचार कीजिए। अभिक्रियकों तथा उत्पादों दोनों ही की सांद्रता 'समय' के साथ चरघातांक से बढती है। निम्नलिखित में से कौन-सा चित्र अभिक्रियकों और उत्पादों की सांद्रता में समय के साथ परिवर्तन की सही व्याख्या करता है?
बहुविकल्प प्रश्न (प्ररूप - II) नोट - निम्नलिखित प्रश्नों में दो या इससे अधिक विकल्प सही हो सकते हैं।
वेग नियम संतुलित रासायनिक समीकरण द्वारा निर्धारित नहीं किया जा सकता यदि ______।
- व्युत्क्रम अभिक्रिया सम्मिलित होती है।
- यह एक प्राथमिक अभिक्रिया हो।
- यह प्राथमिक अभिक्रियाओं की एक शृंखला है।
- कोई भी अभिक्रियक आधिक्य में हो।
एक प्राथमिक अभिक्रिया की संतुलित रासायनिक समीकरण के लिए कौन-से कथन लागू होते है ?
- कोटि, आण्विकता के समान होती है।
- कोटि, आण्विकता से कम होती है।
- कोटि, आण्विकता से अधिक होती है।
- अभिक्रिया की आण्विकता कभी शून्य नहीं हो सकती।
किसी भी एक-अणुक अभिक्रिया के लिए ______।
- दर निर्धारण चरण में केवल एक अभिकारी स्पीसीज प्रयुक्त होती है।
- सबसे धीमे चरण की कोटि तथा आण्विकता एक के बराबर होती है।
- अभिक्रिया की आण्विकता एक होती है और कोटि शून्य होती है।
- अभिक्रिया की आण्विकता और कोटि दोनों ही एक होती हैं।
एक जटिल अभिक्रिया के लिए ______।
- समग्र अभिक्रिया की कोटि सबसे धीमे पद् की आण्विकता के समान होती है।
- समग्र अभिक्रिया की कोटि सबसे धीमे पद् की आण्विकता से कम होती है।
- समग्र अभिक्रिया की कोटि सबसे धीमे पद् की आण्विकता से अधिक होती है।
- सबसे धीमे पद की आण्विकता कभी भी शून्य अथवा अपूर्णांक नहीं होती।
उच्च दाब पर निम्नलिखित अभिक्रिया शून्यकोटि की है।
\[\ce{2NH3 (g) ->[1130 K][\text{प्लैटिनम उत्प्रेरक}] N2(g) + 3H2 (g)}\]
इस अभिक्रिया के लिए कौन-से विकल्प सही है?
- अभिक्रिया का वेग = वेग स्थिरांक
- अभिक्रिया की दर अमोनिया की सांद्रता पर निर्भर करती है।
- अमोनियम के विघटन की दर संपूर्ण अमोनिया विघटित होने तक स्थिर रहेगी।
- दाब में और अधिक वृद्धि अभिक्रिया की दर परिवर्तित कर देगी।
एक सक्रियत संकुल के विघटन के दौरान ______।
- ऊर्जा हमेशा निष्काषित होती है।
- ऊर्जा हमेशा अवशोषित होती है।
- ऊर्जा परिवर्तित नहीं होती।
- अभिक्रियक बन सकते हैं।
ऊर्जा के मैक्सवेल बोल्ट्जमान वितरण के अनुसार ______।
- उच्च तापों पर अधिकतम सम्भाव्य गातिज ऊर्जा प्राप्त अणुओं का अंश घटता है।
- उच्च तापों पर अधिकतम सम्भाव्य गातिज ऊर्जा प्राप्त अणुओं का अंश बढ़ता है।
- उच्च तापों पर अधिकतम सम्भाव्य गतिज ऊर्जा बढ़ती है।
- उच्च तापों पर अधिकतम सम्भाव्य गतिज ऊर्जा घटती है।
ऊजा के वितरण को दशाने वाले मैक्सवेल बोल्ट्जमान द्वारा दिए ग्राफ में ______।
- ताप में वृद्ध के साथ वक्र के अंतर्गत क्षेत्रफल स्थिर रहना चाहिए।
- ताप में वृद्ध के साथ वक्र के अंतर्गत क्षेत्रफल बढ़ता है।
- ताप में वुद्ध के साथ वक्र के अंतर्गत क्षेत्रफल घटता है।
- ताप में वृद्ध के साथ वक्र चौड़ा हो जाता है तथा दाहिनी ओर विस्थापित हो जाता है।
निम्नलिखित में से कौन-सा कथन अरेनियस समीकरण के अनुसार है?
- ताप में वृद्धि के साथ अभिक्रिया का वेग बढता है।
- सक्रियण ऊर्जा में कमी के साथ अभिक्रिया का वेग बढ़ता है।
- ताप में वृद्धि के साथ वेग स्थिरांक में चरघतांकी कमी होती है।
- सक्रियण ऊर्जा में कमी से अभिक्रिया का वेग घटता है।
गलत कथनों को चिह्नित कीजिए।
- उत्प्रेरक अभिक्रिया को वैकल्पिक पथ उपलब्ध कराता है।
- उत्प्रेरक सक्रियण ऊर्जा को बढाता है।
- उत्प्रेरक सक्रियण ऊर्जा को कम करता है।
- उत्प्रेरक अभिक्रिया के एन्थैल्पी परिवर्तन को बदल देता है।
किसी शून्य कोटि की अभिक्रिया के लिए निम्नलिखित में से कौन-से ग्राफ सही हैं?
(i)
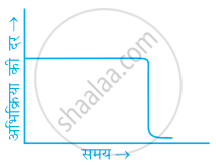
(ii)
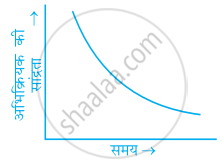
(iii)
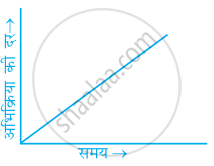
(iv)
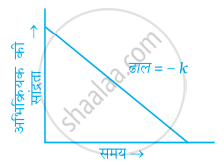
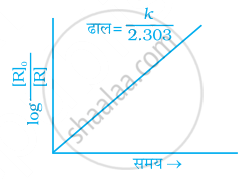
प्रथम कोटी की अभिक्रिया के लिए निम्नलिखित में से कौन-से ग्राफ सही हैं?
(i)
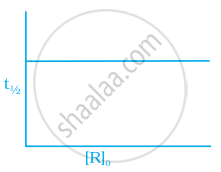
(ii)
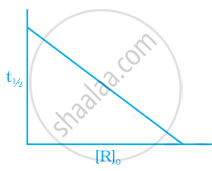
(iii)
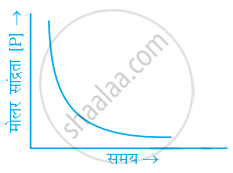
(iv)
लघु उत्तर प्रश्न
एक ऐसी परिस्थिति बताइए जिसमें द्विअणुक अभिक्रिया गतिक रूप से प्रथम कोटि की अभिक्रिया हो।
यदि अभिक्रिया, 2A + B → C शून्य कोटि की हो तो इसके लिए अभिक्रिया वेग लिखिए।
आप निम्नलिखित अभिक्रिया का वेग नियम कैसे निर्धारित कर सकते हैं?
\[\ce{2NO (g) + O2(g) -> 2NO2 (g)}\]
किस प्रकार की अभिक्रियाओं के लिए आणिवकता तथा कोटि के मान समान होते हैं?
एक अभिक्रिया में यदि अभिक्रियक A की सांद्रता तिगुनी कर दी जाए तो अभिक्रिया वेग सत्ताइस गुना बढ़ जाता है। अभिक्रिया की कोटि क्या है?
शून्य कोटि अभिक्रिया के पूर्ण होने में लगने वाले समय के परिकलन के लिए व्यंजक व्युत्पन्न कीजिए।
A + B →उत्पाद, अभिक्रिया के लिए वेग नियम है - दर = k [A] [B]3/2। क्या यह अभिक्रिया एक प्रारंभिक अभिक्रिया है? समझाइए।
अभिक्रिया में अणुओं के बहुत बड़े अंश की ऊर्जा देहली ऊर्जा से अधिक है फिर भी अभिक्रिया वेग बहुत कम है, ऐसा क्यों है?
स्पष्ट कीजिए कि क्या शून्य कोटि अभिक्रिया के लिए अणुसंख्यकता शून्य होगी।
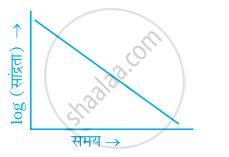
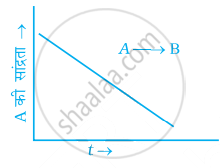
एक सामान्य अभिक्रिया A →B के लिए A की सांद्रता तथा समय के मध्य ग्राफ चित्र में दिया गया है।
- अभिक्रिया की कोटि क्या है?
- वक्र का ढाल क्या है?
- वेग स्थिरांक की इकाई क्या है?
स्पष्ट कीजिए कि H2(g) तथा O2(g) के मध्य अभिक्रिया अति संभाव्य है परन्तु गैसों को एक ही पात्र में कमरे के ताप पर रखने से जल क्यों नहीं बनता।
ताप में वृद्ध से अभिक्रिया वेग क्यों बढ़ता है?
कक्ष ताप पर वायु में ऑक्सीजन प्रचुरता से उपलब्ध होने पर भी ईंधन स्वयं क्यों नहीं जलते?
तीन से अधिक आणिकता वाली अभिक्रियाओं की संभावनाएँ बहुत कम क्यों होती हैं?
सामान्यत:, अभिक्रिया के दौरान अभिक्रिया वेग घटता क्यों है?
किसी अभिक्रिया के लिए केवल ऊष्मागतिक संभाव्यता अभिक्रिया के वेग को निर्धारित नहीं कर सकती। इसे एक उदाहरण की सहायता से समझाइए।
ऑक्सैलिक अम्ल तथा KMnO4 के मध्य ऑक्सीकरण-अपचयन अनुमापन में हम अनुमापन प्रारम्भ करने से पूर्व ऑक्सैलिक अम्ल विलयन को गरम क्यों करते हैं?
किसी अभिक्रिया की आणविकता शून्य क्यों नहीं हो सकती?
आण्विकता केवल प्राथमिक अभिक्रिया के लिए अनुप्रयोज्य क्यों है, जबकि अभिक्रिया की कोटि प्राथमिक तथा जटिल दोनों के लिए अनुप्रयोज्य है?
किसी अभिक्रिया के वेग नियम को हम संतुलित रासायनिक अभिक्रिया की सहायता से निर्धारित क्यों नहीं कर सकते?
सुमेलन प्ररूप प्रश्न
कॉलम I में दिए गए ग्राफ और कॉलम II में दी गई अभिक्रिया की कोटि को सुमेलित कीजिए। कॉलम I के एक से अधिक पद्, कॉलम II के समान पद से संबंधित हो सकते हैं।
| कॉलम I | कॉलम II |
|
(i)
|
|
|
(ii)
|
(a) प्रथम कोटि |
|
(iii)
|
(b) शून्य कोटि |
|
(iv)
|
कॉलम I और कॉलम II में दिए कथनों को सुमेलित कीजिए।
| कॉलम I | कॉलम II |
| (i) उत्प्रेरक अभिक्रिया के वेग को | (a) भिन्नात्मक अथवा शून्य नहीं हो सकती परिवर्तित कर देते हैं। |
| (ii) आण्विकता | (b) हमेशा उपयुक्त अभिविन्यास नहीं होता। |
| (iii) प्रथम कोटि अभिक्रिया की द्वितीय अर्धआयु | (c) सक्रियण ऊर्जा को कम करके |
| (iv) `"e"^(- "E"_"a"//"RT")` | (d) प्रथम के समान होती है। |
| (v) ऊर्जा की दृष्टि से अनुकूल अभिक्रिया कभी-कभी धीमी होती है। | (e) कुल प्रायिकता एक है। |
| (vi) मैक्सवेल बोल्ट्जमान वक्र के अंतर्गत क्षेत्रफल | (f) सक्रियण ऊर्जा के बराबर अथवा उससे स्थिर होता है। अधिक ऊर्जा वाले अणुओं के अंश से संबंधित |
निम्नलिखित का सुमेलन कीजिए-
| कॉलम I | कॉलम II |
| (i) हीरा (डायमण्ड) | (a) समय का लघु अंतराल |
| (ii) तार्क्षणिक वेग | b) सामान्यत: परिवर्तन का वेग परिलक्षित नहीं होता। |
| (iii) औसत वेग | (c) लंबी समयावधि |
कॉलम I और कॉलम II में दिए गए कथनों को सुमेलित कीजिए-
| कॉलम I | कॉलम II |
| (i) अभिक्रिया वेग का गणितीय व्यंजक | (a) वेग स्सिरांक के |
|
(ii) शून्य कोटि की अभिक्रिया के लिए अभिक्रिया |
(b) वेग नियम अभिक्रिया वेग बराबर होता है। |
|
(iii) शून्य कोटि के लिए वेग स्थिरांक की इकाई |
(c) सबसे धीमे चरण की कोटि |
| (iv) एक जटिल अभिक्रिया की कोटि निर्थारित होती है। | (d) अभिक्रिया की दर होती है। |
अभिकथन एवं तर्क प्ररूप प्रश्न
अभिकथन - अभिक्रिया की कोटि शून्य अथवा भिन्नात्मक हो सकती है।
तर्क - संतुलित रासायनिक समीकरण से हम कोटि का निर्धारण नहीं कर सकते।
अभिकथन और तर्क दोनों सही हैं और तर्क अभिकथन का सही स्पष्टीकरण है।
अभिकथन और तर्क दोनों सही कथन हैं परन्तु तर्क अभिकथन का स्पष्टीकरण नहीं है।
अभिकथन सही है परन्तु तर्क गलत कथन है।
अभिकथन और तर्क दोनों ही गलत कथन हैं।
अभिकथन गलत है परन्तु तर्क सही कथन है।
अभिकथन - कोटि एवं आणिवकता एकसमान होती हैं।
तर्क - कोटि का निर्धारण प्रयोग द्वारा होता है तथा आणिवकता वेग निर्धारक प्राथमिक चरण में स्टॉइकियोमितीय गुणांक का योग होती है।
अभिकथन और तर्क दोनों सही हैं और तर्क अभिकथन का सही स्पष्टीकरण है।
अभिकथन और तर्क दोनों सही कथन हैं परन्तु तर्क अभिकथन का स्पष्टीकरण नहीं है।
अभिकथन सही है परन्तु तर्क गलत कथन है।
अभिकथन और तर्क दोनों ही गलत कथन हैं।
अभिकथन गलत है परन्तु तर्क सही कथन है।
अभिकथन - उत्प्रेरक की उपस्थिति में अभिक्रिया की एन्थैल्पी स्थिर रहती है।
तर्क - अभिक्रिया में भाग लेने वाला उत्प्रेरक भिन्न सक्रियण संकुल बनाता है तथा सक्रियण ऊर्जा को कम करता है परन्तु अभिक्रियकों एवं उत्पादों की ऊर्जा समान रहती है।
अभिकथन और तर्क दोनों सही हैं और तर्क अभिकथन का सही स्पष्टीकरण है।
अभिकथन और तर्क दोनों सही कथन हैं परन्तु तर्क अभिकथन का स्पष्टीकरण नहीं है।
अभिकथन सही है परन्तु तर्क गलत कथन है।
अभिकथन और तर्क दोनों ही गलत कथन हैं।
अभिकथन गलत है परन्तु तर्क सही कथन है।
अभिकथन - अभिक्रियक अणुओं के प्रत्येक संघट्ट से उत्पाद बनता है।
तर्क - केवल उन्हीं संघट्टों से उत्पाद निर्माण होता है जिनमें अणुओं का विन्यास सही तथा गतिज ऊर्जा पर्याप्त होती है।
अभिकथन और तर्क दोनों सही हैं और तर्क अभिकथन का सही स्पष्टीकरण है।
अभिकथन और तर्क दोनों सही कथन हैं परन्तु तर्क अभिकथन का स्पष्टीकरण नहीं है।
अभिकथन सही है परन्तु तर्क गलत कथन है।
अभिकथन और तर्क दोनों ही गलत कथन हैं।
अभिकथन गलत है परन्तु तर्क सही कथन है।
अभिकथन - अर्रेनिअस समीकरण से सामान्य तथा जटिल अणुओं के लिए निर्धारित वेग स्थिरांक लगभग परिशुद्ध होते हैं।
तर्क - संघट्ट के समय अभिक्रियक अणुओं का कोई भी अभिविन्यास होने पर भी रासायनिक परिवर्तन हो जाता है।
अभिकथन और तर्क दोनों सही हैं और तर्क अभिकथन का सही स्पष्टीकरण है।
अभिकथन और तर्क दोनों सही कथन हैं परन्तु तर्क अभिकथन का स्पष्टीकरण नहीं है।
अभिकथन सही है परन्तु तर्क गलत कथन है।
अभिकथन और तर्क दोनों ही गलत कथन हैं।
अभिकथन गलत है परन्तु तर्क सही कथन है।
दीर्घ उत्तर प्रश्न
सभी पर्याप्त ऊर्जा धारित संघट्ट रासायनिक परिवर्तन में परिणित नहीं होते इसे एक उदाहरण की सहायता से समझाइए।
ताप बढाने से सक्रियण ऊर्जा तथा सर्वाधिक सम्भाव्य गतिज ऊर्जा पर क्या प्रभाव पड़ेगा?
तत्क्षण वेग और औसत वेग में अन्तर स्पष्ट कीजिए।
एक उदाहरण की सहायता से समझाइए कि छद्म प्रथम कोटि अभिक्रिया से क्या अभिप्राय है?
Solutions for 4: रासायनिक बलगतिकी
![NCERT Exemplar solutions for Chemistry [Hindi] Class 12 chapter 4 - रासायनिक बलगतिकी NCERT Exemplar solutions for Chemistry [Hindi] Class 12 chapter 4 - रासायनिक बलगतिकी - Shaalaa.com](/images/chemistry-hindi-class-12_6:5f2b1b2038084cf381bfa42c826a928c.jpg)
NCERT Exemplar solutions for Chemistry [Hindi] Class 12 chapter 4 - रासायनिक बलगतिकी
Shaalaa.com has the CBSE Mathematics Chemistry [Hindi] Class 12 CBSE solutions in a manner that help students grasp basic concepts better and faster. The detailed, step-by-step solutions will help you understand the concepts better and clarify any confusion. NCERT Exemplar solutions for Mathematics Chemistry [Hindi] Class 12 CBSE 4 (रासायनिक बलगतिकी) include all questions with answers and detailed explanations. This will clear students' doubts about questions and improve their application skills while preparing for board exams.
Further, we at Shaalaa.com provide such solutions so students can prepare for written exams. NCERT Exemplar textbook solutions can be a core help for self-study and provide excellent self-help guidance for students.
Concepts covered in Chemistry [Hindi] Class 12 chapter 4 रासायनिक बलगतिकी are रासायनिक अभिक्रिया वेग, अभिक्रिया वेग को प्रभावित करने वाले कारक, समाकलित वेग समीकरण, अभिक्रिया वेग की ताप पर निर्भरता, अभिक्रिया का रासायनिक संघट्ट सिध्दांत, शून्य कोटि की अभिक्रियाएँ, प्रथम कोटि की अभिक्रियाएँ, अभिक्रिया की अर्धायु, छद्म प्रथम कोटि.
Using NCERT Exemplar Chemistry [Hindi] Class 12 solutions रासायनिक बलगतिकी exercise by students is an easy way to prepare for the exams, as they involve solutions arranged chapter-wise and also page-wise. The questions involved in NCERT Exemplar Solutions are essential questions that can be asked in the final exam. Maximum CBSE Chemistry [Hindi] Class 12 students prefer NCERT Exemplar Textbook Solutions to score more in exams.
Get the free view of Chapter 4, रासायनिक बलगतिकी Chemistry [Hindi] Class 12 additional questions for Mathematics Chemistry [Hindi] Class 12 CBSE, and you can use Shaalaa.com to keep it handy for your exam preparation.