Advertisements
Chapters
2: परमाणु की संरचना
3: तत्त्वों का वर्गीकरण एवं गुणधर्मों में आवर्तिता
4: रासायनिक आबंधन तथा आण्विक संरचना
5: द्रव्य की अवस्थाएँ
6: ऊष्मागतिकी
7: साम्यावस्था
▶ 8: अपचयोपचय अभिक्रियाएँ
9: हाइड्रोजन
10: s-ब्लॉक तत्त्व
11: p-ब्लॉक तत्त्व
12: कार्बनिक रसायन : कुछ आधारभूत सिद्धांत तथा तकनीकें
13: हाइड्रोकार्बन
14: पर्यावरणीय रसायन
![NCERT solutions for Chemistry - Part 1 and 2 [Hindi] Class 11 chapter 8 - अपचयोपचय अभिक्रियाएँ NCERT solutions for Chemistry - Part 1 and 2 [Hindi] Class 11 chapter 8 - अपचयोपचय अभिक्रियाएँ - Shaalaa.com](/images/chemistry-part-1-and-2-hindi-class-11_6:134c1ea964064b77973b84538c3adc59.jpg)
Advertisements
Solutions for Chapter 8: अपचयोपचय अभिक्रियाएँ
Below listed, you can find solutions for Chapter 8 of CBSE NCERT for Chemistry - Part 1 and 2 [Hindi] Class 11.
NCERT solutions for Chemistry - Part 1 and 2 [Hindi] Class 11 8 अपचयोपचय अभिक्रियाएँ अभ्यास [Pages 277 - 280]
निम्नलिखित स्पीशीज में रेखांकित तत्त्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
NaH2PO4
निम्नलिखित स्पीशीज में रेखांकित तत्त्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
NaHSO4
निम्नलिखित स्पीशीज में तत्त्व रेखांकित तत्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
H4P2O7
निम्नलिखित स्पीशीज में रेखांकित तत्त्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
K2MnO4
निम्नलिखित स्पीशीज में रेखांकित तत्त्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
CaO2
निम्नलिखित स्पीशीज में रेखांकित तत्त्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
NaBH4
निम्नलिखित स्पीशीज में रेखांकित तत्त्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
H2S2O7
निम्नलिखित स्पीशीज में रेखांकित तत्त्व की ऑक्सीकरण संख्या का निर्धारण कीजिए-
KAl(SO4)2.12H2O
निम्नलिखित यौगिक के रेखांकित तत्व की ऑक्सीकरण-संख्या क्या है तथा इस परिणाम को आप कैसे प्राप्त करते हैं?
KI3
निम्नलिखित यौगिक के रेखांकित तत्त्व की ऑक्सीकरण संख्या क्या है तथा इस परिणाम को आप कैसे प्राप्त करते हैं?
H2S4O6
निम्नलिखित यौगिक के रेखांकित तत्व की ऑक्सीकरण संख्या क्या है तथा इस परिणाम को आप कैसे प्राप्त करते हैं?
Fe3O4
निम्नलिखित यौगिक के रेखांकित तत्व की ऑक्सीकरण संख्या क्या है तथा इस परिणाम को आप कैसे प्राप्त करते हैं?
CH3CH2OH
निम्नलिखित यौगिक के रेखांकित तत्त्व की ऑक्सीकरण संख्या क्या है तथा इस परिणाम को आप कैसे प्राप्त करते हैं?
CH3COOH
निम्नलिखित अभिक्रिया का अपचयोपचय अभिक्रिया के रूप में औचित्य स्थापित करने का प्रयास कीजिए-
\[\ce{CuO(s) + H2(g) + Cu(s) + H2O(g)}\]
निम्नलिखित अभिक्रिया का अपचयोपचय अभिक्रिया के रूप में औचित्य स्थापित करने का प्रयास कीजिए-
\[\ce{Fe2O3(s) + 3CO(g) → 2Fe(s) + 3CO2(g)}\]
निम्नलिखित अभिक्रिया का अपचयोपचय अभिक्रिया के रूप में औचित्य स्थापित करने का प्रयास कीजिए-
\[\ce{4BCl3(g) + 3LiAlH4(s) -> 2B2H6(g) + 3LiCl(s) + 3AlCl3(s)}\]
निम्नलिखित अभिक्रिया का अपचयोपचय अभिक्रिया के रूप में औचित्य स्थापित करने का प्रयास कीजिए-
\[\ce{2K(S) + F2(g) -> 2K^+F^-(s)}\]
निम्नलिखित अभिक्रिया का अपचयोपचय अभिक्रिया के रूप में औचित्य स्थापित करने का प्रयास कीजिए-
\[\ce{4NH3(g) + 5O2(g) -> 4NO(g) + 6H2O(g)}\]
फ्लुओरीन बर्फ से अभिक्रिया करके यह परिवर्तन लाती है-
\[\ce{H2O(s) + F2(g) -> HF(g) + HOF(g)}\]
इस अभिक्रिया का अपचयोपचय औचित्य स्थापित कीजिए।
H2SO5, \[\ce{Cr2O^{2-}_7}\] तथा \[\ce{NO^-_3}\] में सल्फर, क्रोमियम तथा नाइट्रोजन की ऑक्सीकरण संख्या की गणना कीजिए। साथ ही इन यौगिकों की संरचना बताइए तथा इसमें हेत्वाभास (fallacy) का स्पष्टीकरण दीजिए।
निम्नलिखित यौगिक के सूत्र लिखिए-
मरक्यूरी (II) क्लोराइड
निम्नलिखित यौगिक के सूत्र लिखिए-
निकल (II) सल्फेट
निम्नलिखित यौगिक के सूत्र लिखिए-
टिन (IV) ऑक्साइड
निम्नलिखित यौगिक के सूत्र लिखिए-
थेलियम (I) सल्फेट
निम्नलिखित यौगिक के सूत्र लिखिए-
आयरन (III) सल्फेट
निम्नलिखित यौगिक के सूत्र लिखिए-
क्रोमियम (III) ऑक्साइड
उन पदार्थों की सूची तैयार कीजिए, जिनमें कार्बन -4 से +4 तक की तथा नाइट्रोजन -3 से +5 तक की ऑक्सीकरण अवस्था होती है।
अपनी अभिक्रियाओं में सल्फर डाइऑक्साइड तथा हाइड्रोजन परॉक्साइड ऑक्सीकारक तथा अपचायक दोनों ही रूपों में क्रिया करते हैं, जबकि ओजोन तथा नाइट्रिक अम्ल केवल ऑक्सीकारक के रूप में ही। क्यों?
इन अभिक्रिया को देखिए -
\[\ce{6CO2(g) + 6H2O(l) -> C6H12O6(aq) + 6O2(g)}\]
बताइए कि इन्हें निम्नलिखित ढंग से लिखना ज्यादा उचित क्यों है?
\[\ce{6CO2(g) + 12H2O(l) -> C6H12O6(aq) + 6H2O(l) + 6O2(g)}\]
उपर्युक्त अपचयोपचय अभिक्रिया के अन्वेषण की विधि सुझाइए।
इस अभिक्रिया को देखिए-
\[\ce{O3(g) + H2O2(l) -> H2O(l) + 2O2(g)}\]
बताइए कि इसे निम्नलिखित ढंग से लिखना ज्यादा उचित क्यों है?
\[\ce{O3(g) + H2O2(l) -> H2O(l) + O2(g) + O2(g)}\]
उपर्युक्त अपचयोपचय अभिक्रिया के अन्वेषण की विधि सुझाइए।
AgF2 एक अस्थिर यौगिक है। यदि यह बन जाए, तो यह यौगिक एक अति शक्तिशाली ऑक्सीकारक की भाँति कार्य करता है। क्यों?
"जब भी एक ऑक्सीकारक तथा अपचायक के बीच अभिक्रिया संपन्न की जाती है, तब अपचायक के आधिक्य में निम्नतर ऑक्सीकरण अवस्था का यौगिक तथा ऑक्सीकारक के आधिक्य में उच्चतर ऑक्सीकरण अवस्था का यौगिक बनता है।" इस वक्तव्य का औचित्य तीन उदाहरण देकर दीजिए।
इस प्रेक्षण की अनुकूलता को कैसे समझाएँगे?
यद्यपि क्षारीय पोटैशियम परमैंगनेट तथा अम्लीय पोटैशियम परमैंगनेट दोनों ही ऑक्सीकारक हैं। फिर भी टॉलूईन से बेंजोइक अम्ल बनाने के लिए हम एल्कोहॉलक पोटैशियम परमैंगनेट का प्रयोग ऑक्सीकारक के रूप में क्यों करते हैं? इस अभिक्रिया के लिए संतुलित अपचयोपचय समीकरण दीजिए।
इस प्रेक्षण की अनुकूलता को कैसे समझाएँगे?
क्लोराइडयुक्त अकार्बनिक यौगिक में सांद्र सल्फ्यूरिक अम्ल डालने पर हमें तीक्ष्ण गंध वाली HCI गैस प्राप्त होती है, परंतु यदि मिश्रण में ब्रोमाइड उपस्थित हो, तो हमें ब्रोमीन की लाल वाष्प प्राप्त होती है, क्यों?
निम्नलिखित अभिक्रिया में ऑक्सीकृत, अपचयित, ऑक्सीकारक तथा अपचायक पदार्थ पहचानिए-
\[\ce{2AgBr(s) + C6H6O2(aq) -> 2Ag(s) + 2HBr(aq) + C6H4O2(aq)}\]
निम्नलिखित अभिक्रियाओं में ऑक्सीकृत, अपचयित, ऑक्सीकारक तथा अपचायक पदार्थ पहचानिए-
\[\ce{HCHO(l) + 2[Ag(NH3)2]^+(aq) + 3OH^-(aq) -> 2Ag(s) + HCOO^-(aq) + 4NH3(aq) + 2H2O(l)}\]
निम्नलिखित अभिक्रियाओं में ऑक्सीकृत, अपचयित, ऑक्सीकारक तथा अपचायक पदार्थ पहचानिए-
\[\ce{HCHO(l) + 2Cu^2+(aq) + 5OH^-(aq) -> Cu2O(s) + HCOO^-(aq) + 3H2O(l)}\]
निम्नलिखित अभिक्रिया में ऑक्सीकृत, अपचयित, ऑक्सीकारक तथा अपचायक पदार्थ पहचानिए-
\[\ce{N2H4(l) + 2H2O2(l) -> N2(g) + 4H2O(l)}\]
निम्नलिखित अभिक्रिया में ऑक्सीकृत, अपचयित, ऑक्सीकारक तथा अपचायक पदार्थ पहचानिए-
\[\ce{Pb(s) + PbO2(s) + 2H2SO4(aq) -> 2PbSO4(s) + 2H2O(l)}\]
निम्नलिखित अभिक्रियाओं में एक ही अपचायक थायोसल्फेट, आयोडीन तथा ब्रोमीन से अलग-अलग प्रकार से अभिक्रिया क्यों करता है?
\[\ce{2S2O^2-_3(aq) + I2(s) -> S4O^2-_6(aq) + 2I^-(aq)}\]
\[\ce{S2O^2-_3(aq) + 2Br2(I) + 5H2O(I) -> 2SO^2-_4(aq) + 4Br^-(aq) + 10H^+(aq)}\]
अभिक्रिया देते हुए सिद्ध कीजिए कि हैलोजनों में फ्लुओरीन श्रेष्ठ ऑक्सीकारक तथा हाइड्रोहैलिक यौगिकों में हाइड्रोआयोडिक अम्ल श्रेष्ठ अपचायक है।
निम्नलिखित अभिक्रिया क्यों होती है?
\[\ce{XeO^{4-}_6(aq) + 2F^-(aq) + 6H^+(aq) -> XeO3(g) + F2(g) + 3H2O(l)}\]
यौगिक Na4XeO6 (जिसका एक भाग \[\ce{XeO^{4-}_6}\] है) के बारे में आप इस अभिक्रिया में क्या निष्कर्ष निकाल सकते हैं?
निम्नलिखित अभिक्रियाओं में-
(क) \[\ce{H3PO2(aq) + 4AgNO3(aq) + 2H2O(l) -> H3PO4(aq) + 4Ag(s) +4HNO3(aq) }\]
(ख) \[\ce{H3PO2(aq) + 2CuSO4(aq) + 2H2O(l) -> H3PO4(aq) + 2Cu(s) + 2H2SO4(aq)}\]
(ग) \[\ce{C6H5CHO(l) + 2[Ag(NH3)2)]^+ (aq) + 3OH^-(aq) -> C6H5COO^-(aq) + 2Ag(s) + 4NH3(aq) + 2H2O(l)}\]
(घ) \[\ce{C6H5CHO(l) + 2Cu^2+(aq) + 5OH^-(aq)}\] कोई परिवर्तन नहीं।
इन अभिक्रियाओं से Ag+ तथा Cu2+ के व्यवहार के विषय में निष्कर्ष निकालिए।
आयन-इलेक्ट्रॉन विधि द्वारा निम्नलिखित रेडॉक्स अभिक्रियाओं को संतुलित कीजिए-
\[\ce{MnO^-_4(aq) + I^-(aq) -> MnO2(s) + I2(s)}\] (क्षारीय माध्यम)
आयन-इलेक्ट्रॉन विधि द्वारा निम्नलिखित रेडॉक्स अभिक्रिया को संतुलित कीजिए-
\[\ce{MnO^-_4(aq) +SO2(g) -> Mn^2+(aq) + HSO^-_4(aq)}\] (अम्लीय माध्यम)
आयन-इलेक्ट्रॉन विधि द्वारा निम्नलिखित रेडॉक्स अभिक्रिया को संतुलित कीजिए-
\[\ce{H2O2(aq) + Fe^2+(aq) -> Fe^{3+}(aq) + H2O(l)}\] (अम्लीय माध्यम)
आयन-इलेक्ट्रॉन विधि द्वारा निम्नलिखित रेडॉक्स अभिक्रिया को संतुलित कीजिए-
\[\ce{Cr2O^2-_7 + SO2(g) -> Cr^3+(aq) + SO^2-_4(aq)}\] (अम्लीय माध्यम)
निम्नलिखित अभिक्रिया के समीकरण को आयन-इलेक्ट्रॉन तथा ऑक्सीकरण-संख्या विधि (क्षारीय माध्यम में) द्वारा संतुलित कीजिए तथा इनमें ऑक्सीकारक और
अपचायकों की पहचान कीजिए-
\[\ce{P4(s) + OH^-(aq) -> PH3(g) + HPO^-_2(aq)}\]
निम्नलिखित अभिक्रिया के समीकरण को आयन-इलेक्ट्रॉन तथा ऑक्सीकरण संख्या विधि (क्षारीय माध्यम में) द्वारा संतुलित कीजिए तथा इनमें ऑक्सीकारक और अपचायकों की पहचान कीजिए-
\[\ce{N2H4(l) + CIO^-_3(aq) -> NO(g) + CI^-(g)}\]
निम्नलिखित अभिक्रिया के समीकरण को आयन-इलेक्ट्रॉन तथा ऑक्सीकरण संख्या विधि (क्षारीय माध्यम में) द्वारा संतुलित कीजिए तथा इनमें ऑक्सीकारक और अपचायकों की पहचान कीजिए-
\[\ce{Cl2O7(g) + H2O2(aq) -> ClO^-_2(aq) + O2(g) + H+(aq)}\]
निम्नलिखित अभिक्रिया से आप कौन-सी सूचनाएँ प्राप्त कर सकते हैं-
\[\ce{(CN)2(g) + 2OH-(aq) -> CN-(aq) + CNO-(aq) + H2O(l)}\]
Mn3+ आयन विलयन में अस्थायी होता है तथा असमानुपातन द्वारा Mn2+, MnO2 और H+ आयन देता है। इस अभिक्रिया के लिए संतुलित आयनिक समीकरण लिखिए-
Cs, Ne, I तथा F में ऐसे तत्त्व की पहचान कीजिए, जो केवल ऋणात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
Cs, Ne, I तथा F में ऐसे तत्त्व की पहचान कीजिए, जो केवल धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
Cs, Ne, I तथा F में ऐसे तत्त्व की पहचान कीजिए, जो ऋणात्मक तथा धनात्मक दोनों ऑक्सीकरण अवस्था प्रदर्शित करता है।
Cs, Ne, I तथा F में ऐसे तत्त्व की पहचान कीजिए, जो न ऋणात्मक और न ही धनात्मक ऑक्सीकरण अवस्था प्रदर्शित करता है।
जल के शुद्धिकरण में क्लोरीन को प्रयोग में लाया जाता है। क्लोरीन की अधिकता हानिकारक होती है। सल्फर डाइऑक्साइड से अभिक्रिया करके इस अधिकता को दूर किया जाता है। जल में होने वाले इस अपचयोपचय परिवर्तन के लिए संतुलित समीकरण लिखिए।
इस पुस्तक में दी गई आवर्त सारणी की सहायता से निम्नलिखित प्रश्नों के उत्तर दीजिए-
संभावित अधातुओं के नाम बताइए, जो असमानुपातन की अभिक्रिया प्रदर्शित कर सकती हों।
किन्हीं तीन धातुओं के नाम बताइए, जो असमानुपातन अभिक्रिया प्रदर्शित कर सकती हों।
नाइट्रिक अम्ल निर्माण की ओस्टवाल्ड विधि के प्रथम पद में अमोनिया गैस के ऑक्सीजन गैस द्वारा ऑक्सीकरण से नाइट्रिक ऑक्साइड गैस तथा जलवाष्प बनती है। 10.0 ग्राम अमोनिया तथा 20.00 ग्राम ऑक्सीजन द्वारा नाइट्रिक ऑक्साइड की कितनी अधिकतम मात्रा प्राप्त हो सकती है?
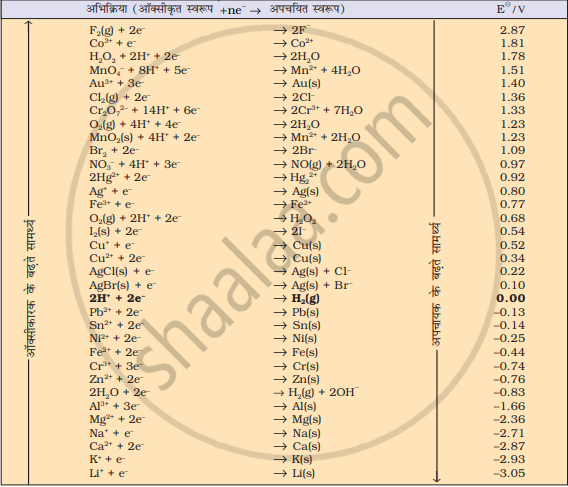
नीचे दिए गए सारणी में मानक विभवों की सहायता से अनुमान लगाइए कि क्या इन अभिकारकों के बीच अभिक्रिया संभव है?
Fe3+ तथा I-(aq)
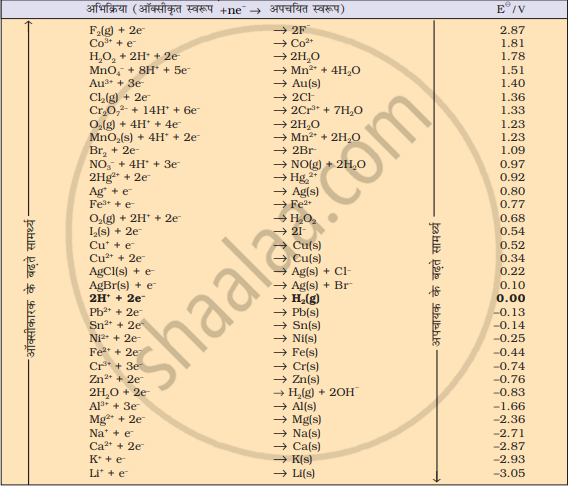
नीचे दिए गए सारणी में मानक विभवों की सहायता से अनुमान लगाइए कि क्या इन अभिकारकों के बीच अभिक्रिया संभव है?
Ag+ तथा Cu(s)
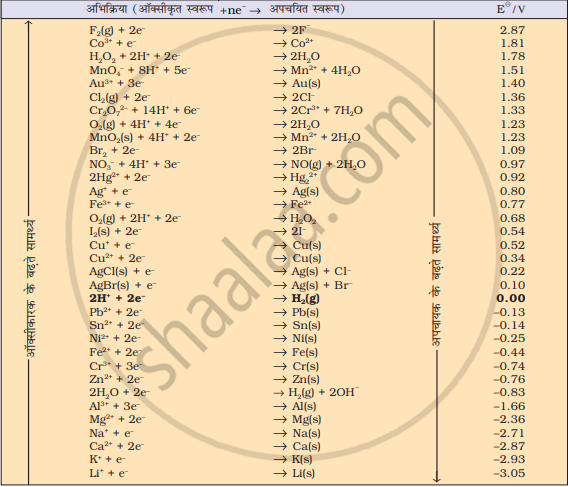
नीचे सारणी में दिए गए मानक विभवों की सहायता से अनुमान लगाइए कि क्या इन अभिकारकों के बीच अभिक्रिया संभव है?
Fe3+(aq) तथा Br−(aq)
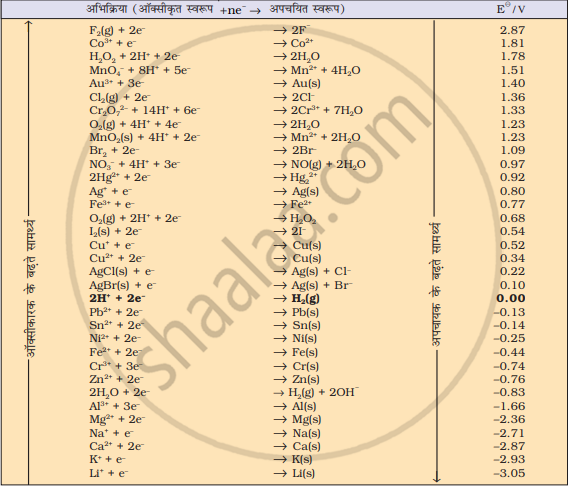
नीचे दिए गए सारणी में मानक विभवों की सहायता से अनुमान लगाइए कि क्या इन अभिकारकों के बीच अभिक्रिया संभव है?
Ag(s) तथा Fe3+(aq)
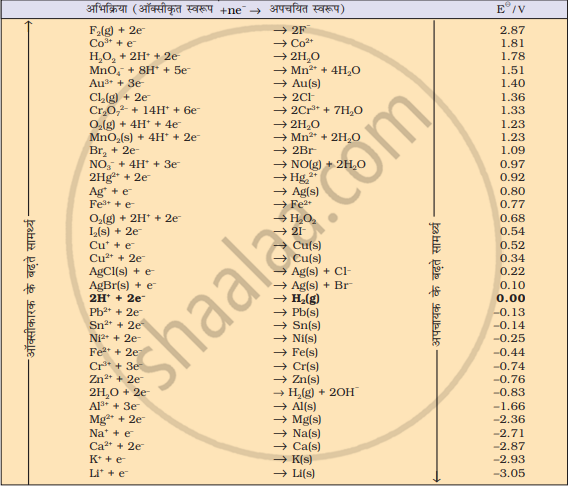
नीचे दिए गए सारणी में मानक विभवों की सहायता से अनुमान लगाइए कि क्या इन अभिकारकों के बीच अभिक्रिया संभव है?
Br2(aq) तथा Fe2+
निम्नलिखित में से विद्युत-अपघटन से प्राप्त उत्पाद के नाम बताइए-
सिल्वर इलेक्ट्रोड के साथ AgNO3 का जलीय विलयन
निम्नलिखित में से विद्युत-अपघटन से प्राप्त उत्पाद के नाम बताइए-
प्लैटिनम इलेक्ट्रोड के साथ AgNO3 का जलीय विलयन
निम्नलिखित में से विद्युत-अपघटन से प्राप्त उत्पाद के नाम बताइए-
प्लैटिनम इलेक्ट्रोड के साथ H2SO4 का तनु विलयन
निम्नलिखित में से विद्युत-अपघटन से प्राप्त उत्पाद के नाम बताइए-
प्लैटिनम इलेक्ट्रोड के साथ CuCl2 का जलीय विलयन
निम्नलिखित धातुओं को उनके लवणें के विलयन में से विस्थापन की क्षमता के क्रम में लिखिए-
Al, Cu, Fe, Mg तथा Zn
नीचे दिए गए मानक इलेक्ट्रोड विभवों के आधार पर धातुओं को उनकी बढ़ती अपचायक क्षमता के क्रम में लिखिए-
K+/K = -2.93 V, Ag+/Ag = 0.80 V, Hg2+/Hg = 0.79 V
Mg2+/Mg = -2.37 V, Cr3+/Cr = -0.74 V
उस गैल्वेनी सेल को चित्रित कीजिए, जिसमें निम्नलिखित अभिक्रिया होती है-
\[\ce{Zn(s) + 2Ag+(aq) -> Zn^2+(aq) + 2Ag(s)}\]
अब बताइए कि-
(क) कौन-सा इलेक्ट्रोड ऋण आवेशित है?
(ख) सेल में विद्युत-धारा के वाहक कौन हैं?
(ग) प्रत्येक इलेक्ट्रोड पर होने वाली अभिक्रियाएँ क्या हैं?
Solutions for 8: अपचयोपचय अभिक्रियाएँ
![NCERT solutions for Chemistry - Part 1 and 2 [Hindi] Class 11 chapter 8 - अपचयोपचय अभिक्रियाएँ NCERT solutions for Chemistry - Part 1 and 2 [Hindi] Class 11 chapter 8 - अपचयोपचय अभिक्रियाएँ - Shaalaa.com](/images/chemistry-part-1-and-2-hindi-class-11_6:134c1ea964064b77973b84538c3adc59.jpg)
NCERT solutions for Chemistry - Part 1 and 2 [Hindi] Class 11 chapter 8 - अपचयोपचय अभिक्रियाएँ
Shaalaa.com has the CBSE Mathematics Chemistry - Part 1 and 2 [Hindi] Class 11 CBSE solutions in a manner that help students grasp basic concepts better and faster. The detailed, step-by-step solutions will help you understand the concepts better and clarify any confusion. NCERT solutions for Mathematics Chemistry - Part 1 and 2 [Hindi] Class 11 CBSE 8 (अपचयोपचय अभिक्रियाएँ) include all questions with answers and detailed explanations. This will clear students' doubts about questions and improve their application skills while preparing for board exams.
Further, we at Shaalaa.com provide such solutions so students can prepare for written exams. NCERT textbook solutions can be a core help for self-study and provide excellent self-help guidance for students.
Concepts covered in Chemistry - Part 1 and 2 [Hindi] Class 11 chapter 8 अपचयोपचय अभिक्रियाएँ are अपचयोपचन अभिक्रियाएँ तथा इलेक्ट्रोड प्रक्रम, अपचयोपचय अभिक्रियाएँ, इलेक्ट्रॉन स्थानांतरण अभिक्रियाओं के रूप में अपचयोपचय अभिक्रियाएँ, ऑक्सीकरण-संख्या, अपचयोपचय अभिक्रियाओं के प्रारूप, अपचयोपचय अभिक्रियाओं का संतुलन, अपचयोपचय अभिक्रियाओं पर आधारित अनुमापन, ऑक्सीकरण अंकधारणा की सीमाएँ, अपचयोपचन अभिक्रियाएँ तथा इलेक्ट्रोड प्रक्रम, अपचयोपचय अभिक्रियाएँ, इलेक्ट्रॉन स्थानांतरण अभिक्रियाओं के रूप में अपचयोपचय अभिक्रियाएँ, ऑक्सीकरण-संख्या, अपचयोपचय अभिक्रियाओं के प्रारूप, अपचयोपचय अभिक्रियाओं का संतुलन, अपचयोपचय अभिक्रियाओं पर आधारित अनुमापन, ऑक्सीकरण अंकधारणा की सीमाएँ.
Using NCERT Chemistry - Part 1 and 2 [Hindi] Class 11 solutions अपचयोपचय अभिक्रियाएँ exercise by students is an easy way to prepare for the exams, as they involve solutions arranged chapter-wise and also page-wise. The questions involved in NCERT Solutions are essential questions that can be asked in the final exam. Maximum CBSE Chemistry - Part 1 and 2 [Hindi] Class 11 students prefer NCERT Textbook Solutions to score more in exams.
Get the free view of Chapter 8, अपचयोपचय अभिक्रियाएँ Chemistry - Part 1 and 2 [Hindi] Class 11 additional questions for Mathematics Chemistry - Part 1 and 2 [Hindi] Class 11 CBSE, and you can use Shaalaa.com to keep it handy for your exam preparation.
